Гам-мет
Cтраница 2
Какой знак должна иметь константа р в уравнении Гам-мета, если реакция облегчается эффектом, снижающим электронную плотность на реакционном центре. [16]
Нуклеофильное замещение в ароматическом ряду удовлетворительно коррелируется обычными константами Гам-мета в тех случаях, когда между заместителем и реакционным центром не возникает достаточно сильного прямого, полярного сопряжения. Однако такое сопряжение может быть весьма существенным. [17]
Определите, коррелируюгся ля эти данные по осиовносгя с помощью уравнения Гам-мета. [18]
Как и следовало ожидать, vCO изменяется симбатно с изменениями значений Гам-мета а, но к интенсивности полос это не относится. Изучено также влияние увеличения числа ароматических циклов. Боуден [186] сообщил значения частот для метиловых эфиров дифенилуксусной кислоты, флуо-рен - и антраценкарбоновых кислот. [19]
Метод определения числа кислотных центров путем титрования их бутиламином с набором индикаторов Гам-мета не дает возможности строго разграничить протонную и апротонную кислотность и не может быть использован для идентификации протонных центров. Этот метод однако пригоден для определения кислотности и относительного распределения кислотных центров по их силе. [20]
Кислотности этой группы кислот не могут быть пока охвачены единым уравнением типа Гам-мета - Тафта. Правда, это является скорее результатом недостаточной разработанности корреляций для реакционных серий с переменным заместителем, поскольку в данном случае мы имеем дело с гидроксильными кислотами типа X-ОН ( № 21 из табл. 3), отличающихся только переменным заместителем X. [21]
Метод определения числа кислотных центров путем титрования их бутиламином с набором индикаторов Гам-мета не дает возможности строго разграничить протонную и апротонную кислотность и не может быть использован для идентификации протонных центров. Этот метод однако пригоден для определения кислотности и относительного распределения кислотных центров по их силе. [22]
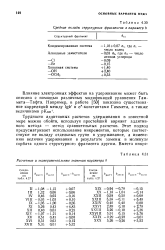 |
Средние вклады структурных фрагментов в параметр b. [23] |
Влияние электронных эффектов на удерживание может быть описано с помощью различных модификаций уравнения Гам-мета - Тафта. [24]
 |
Относительная активность производных толуола к Вг. [25] |
На рис. 12.3 показаны значения для реакции (12.23), которые согласуются с уравнением Гам-мета. [26]
Давно известно, что частоты колебаний ОН-групп мономерных фенолов могут быть сопоставлены с величинами Гам-мета а или значениями рКа заместителей, если только речь не идет об орго-замещении, так как в этом случае стерические эффекты или образование водородной связи могут изменить эти соотношения. Бейкер [23] и Ингольд [26] показали, что частоты колебаний могут быть выражены как функции значений Гаммета а, а Стоун и Томпсон [24] и Браун [25] обнаружили, что это заключение в равной мере относится и к абсолютным интенсивностям. Таким образом, для этого ряда соединений увеличение значения сг, соответствующее увеличению вклада хр2 - состояния атома кислорода, приводит к увеличению полярности группы ОН и уменьшению частоты колебаний. Наиболее сильной кислотой этого ряда является - нитрофенол, который характеризуется наиболее низкой частотой и наиболее высокой интенсивностью поглощения. [27]
Хотя первоначально уравнение Тафта явилось результатом изучения реакционной способности алифатических соединений, а уравнение Гам-мета - ароматических соединений, в ряде последних работ были предложены обобщенные уравнения, которые могут коррелировать экспериментальные данные по реакционной способности соединений любого класса. [28]
На рисунке показана зависимость lg k для реакции диссоциации замещенных уретанов от константы заместителя Гам-мета. [29]
Одним из наиболее старых и, очевидно, наиболее важных корреляционных уравнений этого типа является уравнение Гам-мета. Гаммет установил, что график логарифма константы равновесия ( или скорости) для серии м - и n - замещенных производных бензола представляет собой прямую линию. [30]
Страницы: 1 2 3 4