Гам-мет
Cтраница 3
Одним из наиболее старых и, очевидно, наиболее важных корреляционных уравнений этого типа является уравнение Гам-мета. Гаммет установил, что график логарифма константы равновесия ( или скорости) для серии м - и - замещенных производных бензола представляет собой прямую линию. [31]
Таким образом, мы видим, что все основные типы корреляционных уравнений, по форме аналогичные с уравнением Гам-мета, являются частными случаями уравнения ( III. Следовательно, применимость указанных уравнений ограничивается теми пределами, которые были оговорены при выводе ППЛ и уравнения ( III. Предпосылками использования ППЛ являются в данном случае: 1) непрерывность и монотонность зависимости величин AF для химических реакций от элементарных параметров, связанных со всеми рассмотренными переменными факторами, во всем практически наблюдаемом диапазоне изменения величин Д / 7, и 2) достаточная узость этого диапазона для того, чтобы уравнение ( III. Выполнение этого требования не может быть, на наш взгляд, теоретически обосновано каким-либо независимым путем и нам остается принять его в качестве исходного постулата, введение которого оправдывается соответствующей экспериментальной проверкой. Нам кажется, что материала, цитированного в первой главе данной книги, достаточно для подтверждения справедливости этого постулата. [32]
Для создания абсолютной шкалы кислотности, позволяющей независимо от растворителя и концентрации кислоты количественно оценивать протонирующую способность ее раствора, Гам-мет предложил использовать индикаторный метод. [33]
В общем случае, когда константы скорости k, k - и &2 сравнимы между собой, возможность использования уравнения Гам-мета полностью исключается. [34]
По аналогии с аминами ароматические простые эфиры должны быть значительно менее основны, чем спирты, и вести себя как индикаторы Гам-мета. В основном р / Са эфиров фенолов на структурные изменения реагируют так же, как и р / Са N-алкиланилинов, но они, по-видимому, значительно более чувствительны к стерическому ингибированию резонанса [15, 16] и к стерическим препятствиям сольватации [15], чем их азотные аналоги. [35]
Имеются следующие соображения, которые заставляют с осторожностью относиться к выводам, полученным с помощью проверки связи между константой скорости реакции и функцией Гам-мета и концентрацией протонов. [36]
Аналогично, если на реакционном центре в процессе реакции появляется или исчезает свободная орбиталь, что имеет место при образовании карбкатиона, то заместители, находящиеся в пара-положении и способные проявлять - f - C-эффект, будут обладать большими донорными свойствами, чем в стандартной серии Гам-мета. [37]
Аналогично, если на реакционном центре в процессе реакции появляется или исчезает свободная орбиталь, что имеет место при образовании карбкатиона, то заместители, находящиеся в пара-положении и способные проявлять - j - C-эффект, будут обладать большей донорной способностью, чем в стандартной серии Гам-мета. [38]
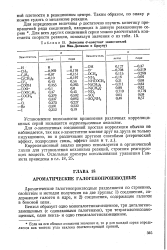 |
Значения 0-констант заместителей ( по Мак-Даниэлю и Брауну. [39] |
Корреляционный анализ широко используется в органической химии для установления механизма реакций, строения реагирующих веществ. Отдельные примеры использования уравнения Гам-мета приведены в гл. [40]
Вскоре выяснилось, что уравнение Гам-мета не всегда соблюдается даже для мета - и лй /) а-замещенных производных бензола. Сам Гаммет указал на это обстоятельство, введя для / шра-нитрогруппы два значения а: нормальное ( 0 78) и завышенное ( 1 27), предназначенное для применения в случае таких реакций, как кислотная диссоциация фенолов и анилиний-ионов. [41]
Таблицы данного раздела предназначены для вычисления констант равновесия и скоростей реакций органических соединений, а также потенциалов полуволн их полярографического восстановления. Таблицы составлены на основании корреляционных уравнений Гам-мета и Тафта и модификаций этих уравнений - см. В. А. Пальм, Успехи химии, 30, вып. Величины, приведенные в табл. 3 - 8, позволяют вычислить около миллиарда значений констант скоростей и равновесия реакций. [42]
Работы Гутинка [5], Тресселта [6], Хасимото Синдзуноби и других авторов [7] посвящены решению ряда теоретических вопросов переменнотоковой полярографии органических веществ. В них показана подчиненность потенциала пика уравнению Гам-мета на переменнотоковых полярограммах органических соединений с различными заместителями; определены константы равновесия различных таутомерных форм; исследованы процессы прото-низации и ряд других теоретических вопросов. В рассмотренных работах аналитические аспекты почти не затрагиваются, и исследований по аналитическому определению органических веществ еще меньше. [43]
Для изучения влияния полярного эффекта лучше всего применять в качестве зонда пара - иди мета-за-мещенные арильные остатки, поскольку при этом заместитель расположен достаточно далеко от места реакции, так что стерический эффект будет снят. Для того чтобы определить поведение заместителей в подобным образом замещенных арильных остатках, Гам-мет оценивал кислотность соответствующих замещенных бензойной кислоты. [44]
Отсюда, зная коэффициенты активности, можно описать с высокой точностью экспериментальные данные, для чего необходимо оптимизировать лишь один параметр - константу ассоциации ионов Mg2 с переходным состоянием. Согласно правилу Олсона - Симонсона, при замене нитрата магния на сульфат наблюдается изменение скорости реакции; Гам-мет представил величину этого изменения как сумму нескольких вкладов, определяемых изменением ионной силы и влипшем последней на константы ассоциации и коэффициенты активности различных частиц, участвующих в реакции. [45]
Страницы: 1 2 3 4