Диазониевый ион
Cтраница 2
Вероятно, наиболее общим является разложение диазониевого иона, но возможно также и термическое разложение N-нитрозоацетанилидов или ароилпероксидов. [16]
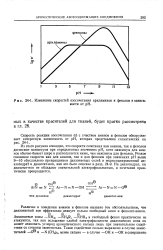 |
Изменение скоростей азосочетания ариламинов и фенолов в зависимости от рН. [17] |
Различие в поведении аминов и фенолов вызвано тем обстоятельством, что диазониевый ион эффективно атакует только свободный амин и фенолят-анион. [18]
В соответствии с теоретическими рассуждениями - / - и - УИ-замести-тели в диазониевом ионе повышают его реакционную способность по отношению к ароматическим соединениям, а группы с / / М - эффектом - понижают ее. [19]
Остюда следует, что большая часть карбониевых ионов, образующихся при отщеплении азота от первоначального диазониевого иона ( гл. [20]
В соответствии с теоретическими рассуждениями - / - и - М - заместители в диазониевом ионе повышают его реакционную способность по отношению к ароматическим соединениям, а группы с / / УИ-эффектом - понижают ее. [21]
Как алифатические, так и ароматические первичные амины реагируют с азотистой кислотой, давая в качестве первоначального продукта соответствующие диазониевые ионы. Как можно было предвидеть, алифатические диазониевые соединения существенно менее стабильны, чем ароматические. Их существование не имеет прямых подтверждений. При распаде они образуют азот, спирт, олефин и другие продукты, а также соединения, получающиеся в результате тех или иных реакций карбониевого иона. На схеме R представляет собой карбониевый ион, образующийся в результате 1 2-перегруппировки. [22]
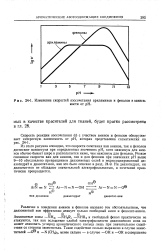 |
Изменение скоростей азосочетания ариламинов и фенолов в зависимости от рН. [23] |
Аммониевые ионы - NHg, - NH2R, - NHR2 и свободный фенол практически не атакуются, так как вследствие слабой электрофильности диазониевого иона он может атаковать углерод ароматического кольца лишь при значительном содействии со стороны заместителя. [24]
Однако в случае простых циклических аминов наиболее последовательная картина может быть получена, если предположить образование обычного ( а не горячего) карбониевого иона как из аксиального, так и из экваториального диазониевого иона и обычное сольволитическое образование экваториального спирта. До тех пор, пока отсутствует более общее объяснение всего разнообразия образующихся продуктов, применение дезаминирования в стереохимических исследованиях ограничивается эмпирическими выводами, Основанными на сравнении с результатами, полученными для аналогичных структур. [25]
Что происходит при дезаминировании амннрв, по-видимому, можно понять с точки зрения модифицированной схемы ионных пар. Положительно заряженный диазониевый ион сильно сольватирован вблизи азота уксусной кислотой. В случае 2-фенилбутила - 2 доминирует атака с фронта, так как сольватация с тыльной стороны третичного бензильпога катиона затруднена. [26]
Вследствие небольшой активности ионов диазония реакция протекает направленно с образованием п - или о-изомеров. Электроно-акцепторные заместители в диазониевом ионе повышают его реакционную способность, а электронодонорные группы понижают ее. [27]
Данные Бенджамина, Шеффера и Коллинза суммированы на приведенной ниже схеме. Слева приведена проекция Ньюмена для диазониевого иона, образующегося из одного из диастереомерньтх меченых аминоспиртов. Кривые стрелки в этой формуле показывают, что, если миграция меченной 14С фенильной группы и отщепление Щ мало разделены во времени, будет образовываться инвертированный продукт и что этот инвертированный продукт образуется за счет миграции только той фенильной группы, которая была меченой. [28]
Этот катион не очень устойчив, поскольку свободная орбиталь находится в плоскости кольца и не может участвовать в делокализации заряда н л-системе. В других реакциях интермедиатом является аддукт нуклеофилз и диазониевого иона. [29]
Этот катион не очень устойчив, поскольку свободная орбиталь находится в плоскости кольца и не может участвовать в делокализацни заряда н л-системе. В других реакциях интермедиатом является аддукт нуклеофила и диазониевого иона. [30]
Страницы: 1 2 3 4