Гаммет
Cтраница 1
Гаммет и Дейрап [71] применили индикаторы с зарядом типа Аг для измерения равновесия реакции ( 22) в водных растворах и затем использовали те же или подобного типа индикаторы для распространения шкалы на другие среды. [1]
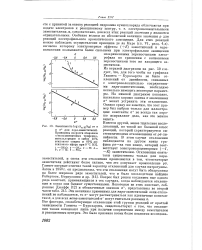 |
Зависимость log ( & п. [2] |
Гаммет впервые отметил такой характер отклонений для случая нитрогуппы. Вопрос был решен созданием еще одного ряда констант, применяющихся в тех случаях, когда наблюдаются отклонения и когда они бывают существенными. Эти величины применимы для / гора-заместителей: если отклонений не наблюдается, то ст - могут рассматриваться как идентичные константам а, а для всех жетеа-заместителей а - могут считаться равными а. Все факторы, способствующие отклонению этой группы реакций от простой зависимости Гаммета - Буркхардта, свидетельствуют о том, что отклонения также возникают лишь при наличии сопряжения между заместителем и реакционным центром. [3]
Гаммет [57], изучая вопросы реакционной способности ароматических соединений, пришел к выводу, что между логарифмом константы скорости той или иной реакции ароматического соединения и константой, характеризующей природу того или иного заместителя, находящегося в пара - или мета-положении к реакционному центру, имеется определенная зависимость, выражаемая уравнением lg / ( po где р-коэффициент, характеризующий данную реакцию, проводимую в данных условиях; о - константа Гаммета данного заместителя. [4]
Гаммет назвал кислотной функцией. [5]
Гаммет наблюдал, что константы скорости реакции алкилирования сложными эфирами возрастают при увеличении кислотности соответствующей кислоты. [6]
Гаммет [6] впервые обратил внимание на то, что относительная реакционная способность галогенид-ионов в воде в 8к2 - реакциях ( см. табл. 5 - 18) обратна их термодинамической стабильности. Так, иодид-ион является наиболее нуклеофильным и также наиболее легко замещаемым из галогенов. [7]
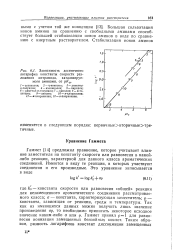 |
Зависимость десятичного логарифма константы скорости разложения нитрамида, катализируемого аминами, от рКа. [8] |
Гаммет [14] предложил уравнение, которое учитывает влияние заместителя на константу скорости или равновесия в какой-либо реакции, характерной для данного класса ароматических соединений. Имеются в виду те реакции, в которых участвуют соединения и его производные. [9]
Гаммет предложил Г55 ] выражать кислотность с помощью так называемой нулевой функции кислотности % Я0, которая является мерой стремления протона кислоты перейти к незаряженной молекуле основания. [10]
Гаммет принял р1 для равновесия ионизации замещенных бензойных кислот. [11]
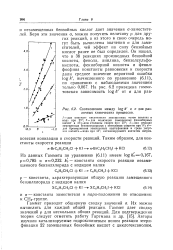 |
Соотношения между log k и а для различных химических процессов. [12] |
Гаммет приводит обширную сводку значений а. [13]
Гаммет [17] предположил, что изменение свободной энергии складывается из изменений энтропии, кинетической энергии и потенциальной энергии. Справедливость этого выражения ограничивается заместителями в пара - и жега-положении бензольного кольца; и во многих реакциях в боковой цепи производных бензола энтропия незначительно изменяется в зависимости от заместителя. Гаммет полагает, что постоянство энтропийного члена подразумевает подобное постоянство в изменении кинетической энергии, и, следовательно, изменение свободной энергии определяется изменением лишь потенциальной энергии. [14]
Гаммет постулировал, что уравнения (1.3) и (1.4) справедливы как для п -, так и для м-замещенных бензольных производных. Более подробный анализ [5, 6] показывает, что в общем случае такое равенство не имеет места. [15]
Страницы: 1 2 3 4