Гаммет
Cтраница 4
Уравнение Гаммета очень полезно с точки зрения теории реакционной способности. Оно показывает, что пропорциональный характер полярных влияний является вполне общим для серии реакций в бензольной системе, которые не затрагивают ни пространственного, ни резонансного эффектов. Уравнение устанавливает важное соотношение между полярными влияниями и строением, а именно аддитивное соотношение. [46]
Константа Гаммета для орто-положения не может быть получена, так как в орто-положении на индуктивный эффект накладывается влияние стерических факторов заместителя. [47]
Константы Гаммета были определены [50-56] для ряда силильных групп. Для сравнения приведены константы некоторых иных заместителей. [48]
 |
Линейность энергий Гельмгольца двух серий реакций ( по данным Сьюббса и Гиншель-вуда ( AF - энергия Гельмгольца активации бензоилирования. [49] |
Уравнение Гаммета плохо применимо к алифатическим соединениям. [50]
Уравнение Гаммета содержит две новые величины - р и а. Константа р характеризует саму реакцию, тип реакции и поэтому называется константой реакционной серии. [51]
Константы Гаммета имеют ограниченное применение, так как они характеризуют суммарное влияние эффектов индуктивного и мезомерного, а на реакционную способность эти эффекты влияют по-разному, особенно при - положении заместителя. [52]
Уравнение Гаммета представляет собой уравнение прямой, и обычно на график наносят по оси абсцисс ст-значения отдельных заместителей, а по оси орди-рмт - - экспериментальные значения Igfe / feo ( рнс. [53]
Правило Гаммета представляет собой простейшую форму проявления полярного эффекта в ароматических соединениях. [54]
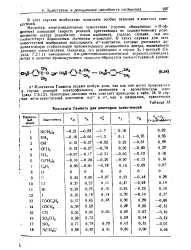 |
Константы Гаммета для некоторых заместителей. [55] |
Константы Гаммета играют особую роль, так как они могут применяться i в случае реакций эле ктроф ильного замещения в ароматическом ядре ( разд. [56]
Страницы: 1 2 3 4