Гаммета
Cтраница 2
Гаммета; с другой стороны, протоны катализируют также и побочные реакции, поэтому выбирают всегда оптимальную концентрацию серной кислоты. [16]
 |
Зависимость констант экстракции ряда элементов от SX и Шро в ряду ТБФ - ТОФО ( ДАМФ-диизоамилметилфосфо-нат. ОДОФ - октилдиоктилфос-финат. [17] |
Гаммета, а еще точнее, что оба метода эквивалентны. [18]
Гаммета, идентичная рН при не очень высокой кислотности. Константа скорости h выражена в мин-1 и относится к реакциям в воде при 25 [ С. [19]
 |
Поляризация теломерных радикалов. [20] |
Гаммета для пара-заместителей; as и ац показывают зависимость скорости данной реакции от полярности заместителей в телогене и мономере; ps и Рм характеризуют реакционную способность телогена и мономера в реакциях с неполярным радикалом. [21]
Гаммета для ароматических соединений) связывает логарифм константы скорости ряда соединений, претерпевающих одинаковые превращения на одном и том же катализаторе с константой заместителя 0, которая характеризует нереагирующую часть молекул. Коэффициент пропорциональности р характеризует как реакцию, так и катализатор; его величина зависит от определения реагирующей и нереагирующей части молекулы и от направления и степени электронных смещений яри образовании активированного комплекса. [22]
Гаммета n - заместителей в бензилга-логениде, которые являются мерой величины электрофильности ( плотности положительного заряда) на реагирующем атоме углерода. [23]
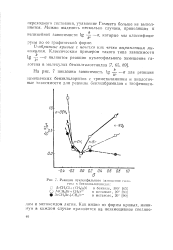 |
Реакции нуклеофильного замещения гало-гегга в бензилгалогенидах. [24] |
Гаммета больше не выполняется. [25]
 |
Расчет константы таутомерного равновесия для системы. [26] |
Гаммета, э скорее наоборот, возникают как результат его выполнения. [27]
Гаммета также может быть применено, однако значение реакционной константы р усложняется. [28]
Гаммета, применяющееся в органической химии для оценки скоростей реакций. [29]
Гаммета, является умение предвидеть и управлять ходом реакций [ 1, с. Такое умение требует знания не только строения и особенностей взаимодействия органических соединений, но также и закономерностей взаимодействия со средой. Из всей массы различных эффектов, входящих в понятие сольватации, часто наиболее важными оказываются слабые специфические взаимодействия - водородные связи между растворителем и реагентами. [30]
Страницы: 1 2 3 4