Гексааммиакат
Cтраница 1
Гексааммиакат ( или гексаммин) Со ( III), полученный по приведенной реакции, имеет оранжевую окраску. [1]
Гексааммиакаты, которые являются производными катионов переходных элементов, почти все без исключения получаются из в о д н ы х р астворов. [2]
 |
Структура бишофита МдС12 - 6Н20. [3] |
Кристаллическая структура гексааммиакатов аналогична структуре гексагидратов. [4]
Для получения гексааммиакатов часто исходят из безводных солей, таких, как PtCl4, СгС13 или NiBr2, подвергая их воздействию газообразного или жидкого аммиака. Во многих случаях получение гексааммиакатов возможно только этим способом, например для Fe3, A13 или Mg2; удобно получать этим путем аммиакаты и других двухвалентных металлов. Иногда газообразным или жидким NH3 медленно действуют на безводную соль. Этот способ эффективен для фторидов металлов [142], так как энергия их решеток выше, чем других галогенидов. [5]
Проведено частичное восстановление гексааммиакатом кальция следующих моноолефинов: З - метилбутена-1, 2-метилбутена - 1, 2-метилбутена - 2, смеси гексена-2 и гексена-3, 2 5-диметилгексена - З и циклогексена. Определены количества образовавшихся предельных углеводородов. [6]
Так как при получении гексааммиаката кальция в реакционном сосуде может остаться некоторое количество непрореагировавшего кальция, а при перегонке продуктов восстановления в результате разложения гексааммиаката кальция под влиянием повышенной температуры может образоваться некоторое количество гидрида кальция, возникает вопрос, не является ли восстановление двойной изолированной связи результатом каталитического действия металлического кальция или гидрида кальция. [7]
Сравнение данных, полученных для гексааммиаката кальция и раствора натрия в жидком аммиаке - систем, способных вызывать перемещение двойных связей в моноолефинах - с данными, полученными для натрия и спирта в жидком аммиаке, показывает, что, хотя вторичная реакция изомеризации несколько меняет результаты первичной реакции восстановления, но не искажает их, и что, следовательно, приведенные в работах Левиной и Казанского с сотрудниками закономерности влияния строения диенов на направление их восстановления сохраняют силу. [8]
Обсужден возможный механизм восстанавливающего действия твердого гексааммиаката кальция. [9]
Значительно легче разрушаются карбонильные соли гексааммиакатов указанных металлов. [10]
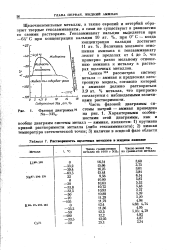 |
Растворимость щелочных металлов в жидком аммиаке. [11] |
Величина мольного отношения аммиака к гексааммиакату лежит в пределах от 4 до 5, что примерно равно мольному отношению аммиака к металлу в растворах щелочных металлов. [12]
Более подробно вплоть до настоящего времени гексааммиакат кальция не изучался, и в современной литературе [36, 37] относительно егр природы сохраняются представления, высказанные Краусом. [13]
Действием аммиака на металлический кальций при охлаждении получают гексааммиакат кальция, который при термическом разложении превращается в. [14]
Щелочноземельные металлы, а также европий и иттербий образуют твердые гексааммиакаты, а сами не существуют в равновесии со своими растворами. Гексааммиакат кальция выделяется при - 64 С при концентрации кальция 10 ат. [15]
Страницы: 1 2 3 4