Гексааммиакат
Cтраница 3
Фирма Dow Chemical Co запатентовала в ряде стран59 90 непрерывное получение безводного хлористого магния высокой чистоты ( 99 5 % MgCl2) путем обработки водного раствора MgCl2 аммиаком в присутствии NH4C1 - выделяющийся гексааммиакат хлорида магния отделяют и подвергают термическому разложению с регенерацией аммиака. Процесс осуществляют в системе реакторов непрерывного действия по двухступенчатой схеме. [31]
Фирма Dow Chemical Co запатентовала в ряде стран89 90 непрерывное получение безводного хлористого магния высокой чистоты ( 99 5 % MgCl2) путем обработки водного раствора MgCl2 аммиаком в присутствии NH, C1 - выделяющийся гексааммиакат хлорида магния отделяют и подвергают термическому разложению с регенерацией аммиака. Процесс осуществляют в системе реакторов непрерывного действия по двухступенчатой схеме. [32]
Хотя большая часть работ выполнена в растворах с переменной ионной силой ( с соответствующей поправкой на коэффициенты активности или без нее), был проведен ряд тщательных исследований комплексов серебра ( I) [7, 8, 15, 55, 58, 60, 63, 75, 80], висмута ( III) [1], таллия ( I) [37, 77] и гексааммиаката кобальта ( III) [53, 54] в постоянной ионной среде. [33]
Щелочноземельные металлы, а также европий и иттербий образуют твердые гексааммиакаты, а сами не существуют в равновесии со своими растворами. Гексааммиакат кальция выделяется при - 64 С при концентрации кальция 10 ат. [34]
Гексамминникель ( П) хлорид [ Ni ( NH3) 6 ] Cl2, гексамминникель ( П) нит-рат [ Ni ( NH3) 6 ] ( NO3) 2, гексамминникель ( П) сульфат [ Ni ( NH3) 6 ] SO4 хорошо растворяются в воде. Некоторые другие гексааммиакаты никеля ( П), такие, как фиолетовый гексамминникель ( Н) бромид [ Ni ( NH3) 6 ] Br, голубой гексамминникель ( П) перхлорат [ Ni ( NH3) 6 ] ( ClC4) 2, в воде малорастворимы. [35]
Для получения гексааммиакатов часто исходят из безводных солей, таких, как PtCl4, СгС13 или NiBr2, подвергая их воздействию газообразного или жидкого аммиака. Во многих случаях получение гексааммиакатов возможно только этим способом, например для Fe3, A13 или Mg2; удобно получать этим путем аммиакаты и других двухвалентных металлов. Иногда газообразным или жидким NH3 медленно действуют на безводную соль. Этот способ эффективен для фторидов металлов [142], так как энергия их решеток выше, чем других галогенидов. [36]
По-видимому, столь же, а может быть, и еще более сильную восстановительную систему, чем натрий - f жидкий аммиак спирт, представляет собой гексааммиакат кальция, который, как уже говорилось, способен восстанавливать и бензол с его гомологами, и диены, и частично мо-ноолефины, причем не только а-олефины, но и олефины иного строения. О структуре и свойствах гексааммиаката кальция ( и других щелочноземельных металлов) до сего времени известно немного. [37]
Аммиакаты трех - и четырехвалентных элементов можно удобно приготовить из аммиакатов двухвалентных катионов осторожным окислением. Однако в присутствии активированного угля превращение СоС12 в гексааммиакат Со3 протекает почти количественно. Из хлоропентаамминовых комплексов Со и Сг удается вытеснять С1 -, действуя аммиаком или аммонийной солью при повышенных температурах и давлении. [38]
Они образуются при действии сухого газообразного аммиака на металлы с поглощением 6 молей аммиака на 1 атом металла, и их существование подтверждается изучением изотерм упругости пара, из которых видно, что соединений с иным количеством молекул аммиака, кроме шести, щелочноземельные металлы не образуют. Скорость разложения гек-сааммиакатов щелочноземельных металлов различная: наиболее стойким является гексааммиакат кальция, легче всего распадается гексаамиакат бария. [39]
С жидким аммиаком щелочноземельные металлы образуют темно-синие растворы. Бильтц ( Biltz, 1920) установил, что существуют только гексааммиакаты, других аммиакатов эти металлы не образуют. [40]
С жидким аммиаком щелочноземельные металлы образуют темно-синие-растворы. Бильтц ( Biltz, 1920) установил, что существуют только гексааммиакаты, других аммиакатов эти металлы не образуют. [41]
С жидким аммиаком щелочноземельные металлы образуют темно-синие растворы. Бильтц ( Biltz, 1920) установил, что существуют только гексааммиакаты, других аммиакатов эти металлы не образуют. [42]
Амид кальция получают растворением металлического кальция в жидком аммиаке и разложением образующегося при этом гексааммиаката. [43]
Колебательный спектр комплексного соединения весьма тонко реагирует на нарушения симметрии последнего. Так, в работе Саккони и Сабатини [13] обнаружено спектроскопическое проявление эффекта Яна - Теллера в гексааммиакате меди. В спектре аммиаката меди в связи со слабым сжатием октаэдра по одной из осей эти полосы расщепляются соответственно на три и две компоненты. Так как ион Мп3 имеет электронную конфигурацию ( 2в) 8 () октаэдрическая симметрия его комплексов должна быть сильно искажена. [44]
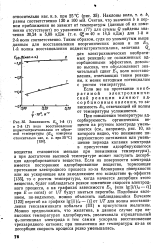 |
Зависимость. д 1 - й ( / и 2 - й ( 2 волн восстановления иодметилтриэтилсилана от обрат-вой температуры (. д измерены относительно нас. к. э. при 25 С [ 134J. [45] |
Страницы: 1 2 3 4