Гексафторацетон
Cтраница 3
Гамбарян и Кнунянц [176] нашли, что диметилбензиламин способен отдавать гидрид-ион гексафторацетону. При этом гидрид-ион неожиданно отрывается не от бензильной, а от метиль-ной группы. [31]
Синтез 3-трифторметил - 1 2 4-триазолов 24 был осуществлен взаимодействием производных иминов гексафторацетона 25 с HN3 с достаточно высокими выходами. [32]
Затем ампулу снова охлаждают до - 78 С, вскрывают, избыток гексафторацетона отгоняют, остаток растворяют в эфире. Эфирный раствор промывают водой, высушивают над MgSCXt; после отгонки эфира остаток перегоняют в вакууме. [33]
Полученные полимеры нерастворимы в органических растворителях - диметилацетамиде, диметилсульфоксиде, гексаме-тилфосфорамиде, сесквигидрате гексафторацетона, муравьиной и трифторуксусной кислотах и полностью или частично растворимы или нерастворимы в серной кислоте. Низкие значения вязкости объясняются прекращением роста цепи в результате снижения растворимости. [34]
Как и в случае диамагнитных фосфонатов с пентакоордина-ционным фосфором, бирадикал 2 присоединяет две молекулы гексафторацетона. [35]
Некоторые производные пиридина могут быть успешно литиированы по положению 2 с использованием в качестве вспомогательного соединения гексафторацетона [49], который образует комплекс с участием неподеленной электронной пары атома азота ( см. разд. На практике простых литиевых производных пиридина используют реакции обмена металл - галоген, однако в присутствии атомов хлора, фтора или других заместителей, способствующих ор / ио-металлированию, возможно литиевых производных методом прямого металлирования ( разд. [36]
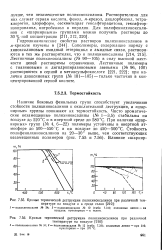 |
Кривые термической деструкции полихиноксалинов при различной температуре на воздухе и в среде гелия.| Кривые термической деструкции полихиноксалинов при различной. [37] |
Растворителями для них служат серная кислота, фенол, ж-крезол, дихлорбензол, тетра-хлорэтан, хлороформ, сесквигидрат гексафторацетона, гексафтор-изопропанол, нитробензол и пиридин. [38]
Нингидрин, как и другие кетоны с сильными акцепторными группами у карбонила, существует в гидратной форме ( см. гексафторацетон - разд. [39]
Этот же замещенный оксйамид образуется в качестве побочного продукта в реакции циклогексена и брома с аддуктом фтористого цезия и гексафторацетона в ацетонитриле. [40]
Нитрит оксима гексафторацетона - легколетучая прозрачная коричневая жидкость с резким запахом окислов азота, легко гид-ролизуется водой до оксима гексафторацетона. [41]
Аддукт можно получать прямо в ампуле для съемки спектра, так как реакция проходит за несколько минут, а избыток гексафторацетона не мешает определению. [42]
В раствор 4 г LiAlH4 в 100 мл абсолютного тетрагидрофурана медленно пропускают 15 ли ( при - 78 С) гексафторацетона при перемешивании. Скорость подачи гексафторацетона регулируют таким образом, чтобы температура реакционной смеси не превышала 50 С. Органический слой отделяют, дважды промывают водой, сушат над силикагелем и перегоняют. [43]
К 150 мл концентрированной H2SO4 при хорошем охлаждении порциями прибавляют 30 г ( 0 13 моль) калиевой соли циангидрина гексафторацетона. Смесь кипятят с обратным холодильником в течение 24 ч при температуре масляной-бани 160 - 180 С, затем перегоняют. [44]
Смесь 16 г ( 0 0935 моль) и-толуолсульфамида, 50 мл абсолютного тетрагидрофурана, 16 г ( 0 096 моль) гексафторацетона и нескольких капель пиридина встряхивают в запаянной ампуле до полного растворения осадка и затем выдерживают при комнатной температуре 2 дня. Содержимое ампулы переносят в перегонную колбу, тетрагидрофуран отгоняют в вакууме водоструйного насоса при температуре не выше 20 С. Затем бензол и избыток хлористого тионила отгоняют в вакууме. Полученный неочищенный N - n - толуолсульфонилимин гексафторацетона растворяют в 100 мл абсолютного эфира. Затем в раствор барбо-тируют при периодическом охлаждении ледяной водой 5 мл ( при - 78 С) кетена. Смесь выдерживают при комнатной температуре в течение 1 ч, затем прибавляют при охлаждении 10 мл спирта. [45]
Страницы: 1 2 3 4