Кислородный ион
Cтраница 1
Кислородный ион во многих фтороксисолях может замещаться или превращаться в ион О - при обработке растворов этих солей перекисью водорода. [1]
Кислородный ион в активированном состоянии ( на вершине потенциального барьера) может вновь забирать электрон у любого из окружающих его двухвалентных ионов с образованием дырочного комплекса. [2]
Кислородные ионы расположены двумя слоями в гексагональной плотнейшей упаковке с размещением между ними катионов алюминия. Каждый катион находится в шестерном окружении ионов кислорода, а каждый ион кислорода в четверной координации А18 ионов. Взаимоплотная упаковка ионов кислорода с ионами алюминия обусловливает значительную прочность структуры корунда. [3]
 |
Зависимость толщины оксида кремния от времени окисления во влажном кислороде при различном содержании водяного пара. [4] |
Кислородные ионы и силаноловые группы в процессе окисления во влажном кислороде диффундируют через оксид и взаимодействуют с поверхностью кремния независимо друг от друга. [5]
Кислородные ионы, войдя в окиснув пленку со стороны раствора под влиянием электрического поля, уже не могут выйти из нее, а могут лишь адсорбироваться на поверхности металла под пленкой, так как с противоположной стороны пленка примыкает к металлу. Поэтому избыточные сверх адсорбированного количества кислородные ионы накапливаются в пленке и уменьшают в ней число анионных вакансий. Одновременно в силу требования электронейтральности в пленке удерживается дополнительное количество катионов и уменьшается число катионных вакансий. Все это приводит к общему уменьшению дефектности пленки и ее проницаемости для катионов и анионов. При этом роль пленки возрастает и наряду с адсорбционной возникает также и пленочная пассивность металла. Здесь еще раз сказывается ионный характер пассивирующего кислорода, что и приводит к уменьшению анионных и катионных вакансий в пленке. Мы видим, что в результате воздействия ионов 0 - при потенциале пассивации возникают адсорбционная и пленочная пассивность, которые сопутствуют друг другу. [6]
Кислородные ионы, потерявшие электроны, захватывают их у ионов трехвалентного церия, а затем образовавшиеся, а также присутствовавшие в стекле ионы четырехвалентного церия захватывают электроны как из зоны проводимости, так и из электронных центров захвата. Первый процесс сопровождается излучением, второй, по-видимому, проходит без него. [7]
Кислородные ионы в соединении ИОН так сильно поляризованы, что не только располагаются слоямв без непосредственного взаимодействия с ионами лития, но даже два слоя, образовав ные ионами кислорода или гидроксила, располагаются один за другим. Так как возникновение слоистых решеток связано с сильной поляризацией, то такие структуры образуются главным образом у соединений, в которых катион не обладает строением инертного газа. Они присущи преимущественно соединениям элементов побочных подгрупп периодической системы, но встречаются и в главных подгруппах ( например. [8]
Кислородные ионы в соединении LiOH так сильно поляризованы, что не только располагаются слоям без непосредственного взаимодействия с ионами лития, но даже два слоя, образован ные ионами кислорода или гидроксила, располагаются один за другим. Так как возникновение слоистых решеток связано с сильной поляризацией, то такие структуры образуются главным образом у соединений, в которых катион не обладает строением инертного газа. [9]
С-О отрицательно заряженный кислородный ион относительно устойчив, в то время как С очень неустойчив и очень реакционноспособен. Окислители и восстановители классифицируются аналогичным образом. [10]
Рефракцию кислородного иона в стеклах наиболее удобно исследовать на основе изучения оптических свойств простых стеклообразных систем. [11]
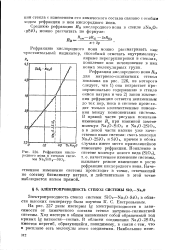 |
Рефракция кислородного иона в стеклах системы Na2Si03 - Si02. [12] |
Рефракцию кислородного иона можно рассматривать как чувствительный индикатор, способный отмечать внутримолекулярные перегруппировки в стеклах, появление или исчезновение в них новых молекулярных групп. [13]
Рефракцию кислородного иона в стеклах наиболее удобно исследовать на основе изучения оптических свойств простых стеклообразных систем. Примеры такого рода исследований даны в разделе, посвященном описанию свойств простых силикатных систем ( см. стр. [14]
 |
Рефракция кислородного иона в стеклах системы SiOj - Na2SiOs. [15] |
Страницы: 1 2 3 4 5