Кислородный ион
Cтраница 2
Рефракцию кислородного иона можно рассматривать как чувствительный индикатор, способный отмечать внутримолекулярные перегруппировки в стеклах, появление или ла исчезновение в них новых молекулярных групп. Рефракция кислородного иона Rо для натриево-силикатных стекол показана на рис. 206, из которого следует, что 1) она возрастает пропорционально содержанию в стекле окиси натрия и что 2) закон изменения рефракции остается неизменным до тех пор, пока в системе происходят количественные изменения между компонентами системы. Качественное изменение системы происходит в точке, отвечающей по составу би-силикату натрия, и действительно в этой точке наблюдается излом прямой. [16]
Рефракция кислородного иона Ло для натриево-силикатных стекол показана на рис. 226, из которого следует, что 1) она возрастает пропорционально содержанию в стекле окиси натрия и что 2) закон изменения рефракции остается неизменным до тех пор, пока в системе происходят только количественные изменения между компонентами системы. В правой части рисунка показано изменение R0 при взаимной замене молекул Na20 - Si02 и Na20 - 2Si02, а в левой части налицо уже качественно иная система: смесь молекул Na20 - 2Si02 nSi02, причем в обоих случаях имеет место прямолинейное-изменение рефракции. Появление в системе молекул нового вида ( Si02), т.е. качественное изменение системы, вызывает резкое изменение в росте рефракции кислородного иона. Качественное изменение системы происходит в точке, отвечающей по составу бисиликату натрия, и действительно в этой точке наблюдается излом прямой. [17]
Так как кислородные ионы являются плотноупакованными в решетке перовскита, возможность введения того или иного числа анионов маловероятна. Присутствие ионов Ti3 вместе с Ti4 должно было бы привести к увеличению удельной электропроводности. [18]
Прибавление доноров кислородных ионов, например Na2O2, усиливает ингибирование электродной реакции. [19]
Прежде всего этот кислородный ион представляет собой одно целое, в то время как двойная связь в Ш3 0 принадлежит не одному кислороду, а является совокупностью пяти кислородных связей 2 / 3, Vsi Vs. Кислородный ион благодаря большой прочности связи ( равной единице) с Ni3 при колебательном движении имеет возможность более близко подойти к Ш3 и сравнительно легко обменяться зарядом. Это приводит к образованию активированного комплекса со сравнительно малой энергией, в который входит нестабильный одновалентный ион кислорода. Такой кислород способен захватить электрон у любого из окружающих его ионов Ni24 с образованием вновь дырочного комплекса той или иной Ориентации. Такой же способностью обладают и другие ионы кислорода, однако при этом требуется большая энергия активации. [20]
Известно, что кислородные ионы и гидроксильные группы в анионах типа OgXOH - 1 - ( X - Si, P, S, Ge) обладают соответственно основными ( электрондонорными) и кислотными протондонорными) свойствами. В силу этого обстоятельства структурными единицами безводных кислых солей являются не отдельные анионы, а более или менее сложные анионные комплексы. [21]
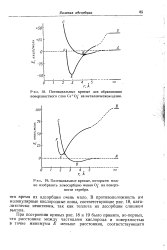 |
Потенциальные кривые для образования поверхностного слоя Cs O T на металлическом цезии.| Потенциальные кривые, которыми можно изобразить хемосорбцию ионов О % на поверхности серебра. [22] |
В противоположность им молекулярные кислородные ионы, соответствующие рис. 18, каталитически неактивны, так как теплота их десорбции слишком высока. [23]
 |
Значения энергий смешения для некоторых стеклообразных систем. [24] |
Состояние электронных оболочек кислородных ионов зависит и от вхождения в состав анионной матрицы стекла других оксидов - стеклообразователей и модификаторов. [25]
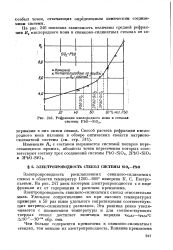 |
Рефракция кислородного иона в стеклах системы РЬО - SiO2. [26] |
Способ расчета рефракции кислородного иона изложен в обзоре оптических свойств натриево-силикатной системы ( см. стр. [27]
Реакция водорода с кислородными ионами решетки, идущая при 800 с выделением воды и затрагивающая частично объем при более низких температурах ( 300 - 600), протекает не так глубоко и очевидно создает лишь поверхностные гидроксильные структуры предварительно дегидратированного образца. [28]
 |
Островные кремнекислородные радикалы. [29] |
Тетраэдры, соединяясь через кислородные ионы, образуют различные сочетания или типы структур: островные, цепные, ленточные, листоватые ( слоистые), каркасные. Каркасная структура распространена в полевых шпатах, кварце, цепная - в пироксенах, листоватая - в слюдах, глинистых минералах, ленточная - в амфиболах, островная - в оливине. [30]
Страницы: 1 2 3 4 5