Кислородный ион
Cтраница 3
 |
Профили концентрации в пленке при стационарном состоянии. [31] |
Вторая стадия представляет собой образование кислородных ионов при взаимодействии адсорбированного кислорода с электронами, которые поступают из объема металла. Третья стадия - быстрая реакция указанных ионов с анионами цинка, которые образовались на границе раздела металл - - оксид и затем продиф-фундировали через слой оксида. [32]
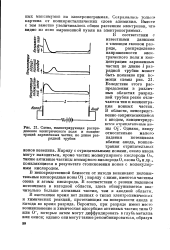 |
Схема, иллюстрирующая распределение электрического поля и концентраций заряженных частиц по длине разрядной трубки. [33] |
В непосредственной близости от катода возникают положительные кислородные ионы 0; наряду с ними, имеются частицы озона и атомы кислорода. В соответствии с резким падением потенциала в катодной области, здесь обнаруживается значительно больше активных частиц, чем в анодной области. [34]
Это сопровождается появлением соответствующего числа вакансий кислородного иона. Наблюдаемое увеличение электропроводности объясняется миграцией кислородных ионов по механизму вакансий. При таких высоких концентрациях А203 в число вакансий будут входить вакансии ближайших соседей, и взаимодействие дефектов в этом случае становится заметным. Было бы интересно измерить удельную электропроводность при пониженных концентрациях добавки. [35]
 |
Изменение дисперсии пр-пс натриево-силикатного стекла. а - при замещении в нем Na2O на MeO ( SiO2 постоянно. б-при замещении в нем SiOj на MeO ( Na2O постоянно. [36] |
Интересно проследить за ходом изменения рефракции кислородного иона в стеклах натриево-силикатной системы. [37]
Следует думать, что при разряде кислородного иона на поверхности Ni203 должен возникать высший окисел никеля, например, по схеме Ni203 - j - 0 - - е - Ni204 и что вся эта суммарная стадия и является замедленной стадией анодного процесса. Такое предположение ничего не меняет во всех приведенных количественных выводах. В этом случае выделение кислорода является уже следствием распада N 204 и должно совершаться быстро. [38]
Следовательно, уменьшение рН при восстановлении сложных кислородных ионов всегда способствует возрастанию их окислительной способности. [39]
Гарнера возникает в результате взаимодействия с кислородными ионами решетки окисла. [40]
Первый и пятый корни учитывают колебания цепочки кислородных ионов. [41]
Высокая концентрация кислородных вакансий обусловливает легкость переноса кислородных ионов через электролит. [42]
 |
Октаэдрические ( О и тетраэдрические ( Г пустоты между атомами при плот-нейшей их упаковке.| Изображение структуры при помощи координационных полиэдров. [43] |
Добавим к этому, что при радиусе кислородного иона 1 35 А размер октаэдрической пустоты получается равным 1 35X0 410 56 А. Поэтому-нет ничего удивительного в том, что в этих пустотах находится место для иона А13, радиус которого равен 0 57 А. [44]
Предполагаемой особенностью структуры фосфатных стекол является наличие односторонне поляризованных кислородных ионов. Такие ионы возникают благодаря структуре тетраэдра Р04, где пятивалентный ион фосфора связан только с четырьмя ионами кислорода, отсюда один ион кислорода должен быть связан с ионом фосфора двумя связями. [45]
Страницы: 1 2 3 4 5