Гексафторфосфат
Cтраница 3
Катион хлорциклопентадиенил-бензолжелеза был выделен в виде боро-фторида и гексафторфосфата. [31]
Ряд рацемических аминокислот в виде солей ( перхлоратов или гексафторфосфатов) удалось успешно разделить на этом сорбенте, используя в качестве растворителя смеси хлороформа с ацетонитрилом. Известен один пример применения афин-ной хроматографии для разделения аминокислот. Триптофан удалось разделить на колонке с агарозой, к которой с помощью сук-циноиламиноэтильного мостика присоединен сывороточный альбумин быка. [32]
К анализируемому раствору, содержащему 36 - 55 мг гексафторфосфата калия, добавляют до щелочной реакции гидроксид аммония. Конечная концентрация аммония должна быть в интервале 5 - 11 М, общий объем раствора - 50 мл. Раствор нагревают до 50 С и медленно, при постоянном перемешивании, добавляют двойной избыток 0 015 М раствора хлорида тетрафениларсония. Через 30 мин осадок отфильтровывают через пористый стеклянный фильтр и промывают 50 мл разбавленного раствора гидроксида аммония порциями по 5 - 10 мл. [33]
В некоторых случаях лучшие выходы фторароматических производных получаются при термическом разложении гексафторфосфатов [3], антимонатов или арсенатов [4] арилдиазония. [34]
С целью получения гидрофобных диазосмол анион ZnCl конденсата л-диазодифениламина с формальдегидом заменяют анионами гексафторфосфата [ пат. Великобритании 1583464 ], тиоциа-ната, дихромата, фторобората, фосфомолибдата; кислот с длинной углеродной цепью: бензол -, n - толуол -, мезитилен -, нафталин -, бу-тилнафталин -, пропилнафталинсульфокислот, часто 2-гидрокси - 4-метоксибензофенон - 5-сульфокислоты [ например, пат. Великобритании 2057704 ], а также 5-сульфосалициловой, 5-сульфокрезотино-вой, додецилбензолсульфокислоты и др. [ пат. [35]
Нитронная соль гексафторфосфорной кислоты была использована Ланге и Мюллером для получения и изучения гексафторфосфатов. При разложении соли водным аммиаком был получен гексафторфосфат аммония; из этой соли были приготовлены другие соединения. Соли щелочных металлов были получены при упаривании досуха растворов аммонийной соли, к которым предварительно были добавлены рассчитанные количества соответствующих гидроокисей. При смешении легко растворимых солей металлов с гексафторфосфатом аммония и амином были получены металл-аминные комплексные соединения. [36]
С целью получения гидрофобных диазосмол анион ZnCljT конденсата л-диазодифениламина с формальдегидом заменяют анионами гексафторфосфата [ пат. Великобритании 1583464 ], тиоциа-ната, дихромата, фторобората, фосфомолибдата; кислот с длинной углеродной цепью: бензол -, - толуол -, мезитилен -, нафталин -, бу-тилнафталин -, пропилнафталинсульфокислот, часто 2-гидрокси - 4-метоксибензофенон - 5-сульфокислоты [ например, пат. Великобритании 2057704 ], а также 5-сульфосалициловой, 5-сульфокрезотино-вой, додецилбензолсульфокислоты и др. [ пат. [37]
Водный слой после обработки гексафторфосфатом натрия дал 2 07 г ( 37 %) гексафторфосфата кобальтициния, который при хроматографии в тонком слое на А1203 ( ацетон) дает только одно желтое пятно, совпадающее с пятном заведомого гексафторфосфата кобальтициния. [38]
Температура поднимается, поэтому смесь охлаждают до - 5 С, чтобы добиться полного осаждения желтого гексафторфосфата диазония. [39]
Выделение гексафторфосфатов осуществляется растворением продукта реакции в воде и осаждением нитронной соли с последующим превращением этой соли в гексафторфосфат аммония. [40]
Как следует из табл. 13.1 и 13.2, достижение предельно высоких анодных потенциалов, помимо использования тетрафтор-боратов и гексафторфосфатов, возможно при понижении температуры [59] или при использовании таких растворителей, как трифторуксусная [60, 67, 68] и фторсульфоновая [57, 69-72] кислоты. Наблюдавшиеся потенциалы в случае необратимого окисления постоянны, и их можно предсказать. Во многих случаях эти потенциалы хорошо коррелируют с потенциалами ионизации [56, 58, 74] и с константами о [63, 64]; в последнее время потенциалы ионизации обычно измеряют методом фотоэлектронной спектроскопии. Общая тенденция изменения потенциалов окисления может быть выведена исходя нз структур углеводородов на основе механизма, включающего перенос электрона с последующим быстрым разрывом связей углерод-водород или углерод-углерод Для таких случаев на наблюдаемый потенциал влияет скорость последующей реакции. С этим связаны относительно низкие потенциалы окисления напряженных углеводородов, катнои-радикалы которых, как можно ожидать, способны подвергаться фрагментации ( см табл 13 4) Таким же образом можно объяснить низкий потенциал окисления цикло-гексадиена-1 4 ( см. табл. 13.3); в этом случае быстрое отщепление протона катион-радикалом приводит к цнклогексаднениль-ному радикалу. [41]
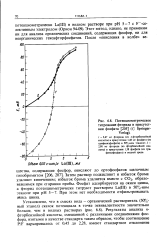 |
Потенциометрическое титрование фторида в присутствии фосфата ( Springer-Verlag. [42] |
Этот метод, однако, не применим ни для анализа органических соединений, содержащих фосфор, ни для неорганических гексафторфосфатов. [43]
Установлено, что в димерном катионе [ СБН5Мо ( ЗМе) 2 ] 2, полученном окислением нейтрального димера и выделенного в виде гексафторфосфата. [44]
К нагретому до 50 С раствору 5 г H2L171 ( см. методику 13) в 800 мл ацетонитрила медленно прибавляют раствор 8 3 г гексафторфосфата n - хлорфенилдиазония в 125 мл ацетонитрила. Одновременно с добавлением раствора диазониевой соли к реакционной смеси медленно вливают раствор, содержащий 20 мл триэтиламина. Образовавшийся темно-красный раствор выдерживают 2 ч при комнатной температуре. Выпавший желтый кристаллический продукт отфильтровывают, промывают ацетонитрилом и высушивают на воздухе. [45]
Страницы: 1 2 3 4