Общий ион
Cтраница 1
Общие ионы, однако, не приводят к проявлению специфического эффекта. [1]
Общими ионами у всех водных растворов щелочей являются гидроксильные ионы, которые и определяют общие свойства щелочей. Если устранить гидроксильные ионы из раствора щелочи, например реакцией нейтрализации, то и щелочные свойства раствора исчезнут. [2]
Влияние общего иона может быть очень большим в случае почти нерастворимых солей. В 0 1 М растворе NaCl растворимость составляет только 1 7 - 10 9 М, что равно лишь 1 / 10 000 доле приведенной выше величины. Отсюда видно, что влияние общего иона можно использовать для полного удаления из раствора ионов серебра ( если не считать следов этих ионов) путем повышения концентрации хлорид-иона. [3]
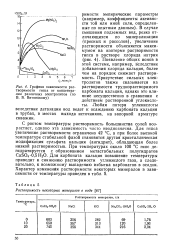 |
Графики зависимости растворимости гипса от концентра -. ции различных электролитов ( по В. В. Витвицкому. [4] |
Появление общих ионов в этой системе, например, вследствие добавления хлорида кальция, более чем на порядок снижает растворимость. Присутствие сильных электролитов также сказывается на растворимости труднорастворимого карбоната кальция, однако это влияние несущественно в сравнении с действием растворенной углекислоты. Любая потеря углекислоты вследствие дегазации вод ведет к осаждению карбоната кальция в трубах, в местах выхода источников, на запорной арматуре скважин. [5]
Влияние общего иона имеет большое значение при весовом анализе, когда почти полностью высаживается какое-либо вещество. [6]
Добавление общего иона может привести к меньшему понижению температуры затвердевания растворов CdCl2, чем вычисленное для простой частицы; это указывает на образование комплексного аниона, содержащего кадмий и хлор. [7]
Влияние общего иона ( разд. [8]
Любая добавка общих ионов согласно уравнению произведения растворимости резко сказывается па равновесие системы, уменьшая растворимость соли. [9]
 |
Зависимость растворимости осадков от избытка осадителя. 4. [10] |
При избытке общего иона растворимость осадка сначала уменьшается. При большом избытке общего иона образование комплексных соединений становится доминирующим процессом и растворимость осадка повышается. [11]
 |
Зависимость растворимости осадков от избытка осадителя. [12] |
При избытке общего иона растворимость осадка сначала уменьшается. При большом избытке общего иона образование комплексных соединений становится доминирующим процессом и растворимость осадка повышается. [13]
Соль с общим ионом не способна вызвать такого эффекта. Однако соль с общим ионом может промотировать стадию ( - 3) и, таким образом, ингибировать сольволиз, проходящий через стадию диссоциации на ионы. [14]
Итак, присутствие общего иона существенно понижает растворимость. [15]
Страницы: 1 2 3 4