Агаровый гель
Cтраница 4
Обычно иммуноэлектрофорез проводят в слое агарового геля на стеклянных пластинках размером 180 х 130 мм, которые следует перед опытом тщательно вымыть, обезжирить, высушить и расположить строго горизонтально; любое отклонение пластинки от горизонтального уровня приводит к неравномерности толщины агарового геля. Рекомендуется применять следующий прием: стеклянную кювету соответствующего размера заполняют 5 % - ным расплавленным агаром; после его затвердения образуется горизонтальная поверхность, на которую и помещают стеклянную пластинку. Для того чтобы положение пластинки всегда было строго горизонтальным, после затвердения агара кювету не следует сдвигать с места. [46]
После внесения исследуемых образцов агаровые пластинки помещают в камеру прибора для электрофореза. Контакт агарового геля с буферными ваннами прибора осуществляется с помощью полосок фильтровальной бумаги, смоченных буферным раствором. Бумажные фитили должны примерно на 15 мм покрывать гель на обоих концах агаровой пластинки. [47]
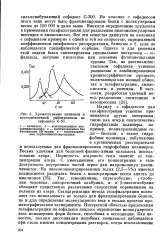 |
Хроматограмма нативной и. [48] |
Пористость агарового геля зависит от концентрации агара. С уменьшением его концентрации в геле доступность внутренних частей зерен для макромолекул увеличивается. Так, гемоцианины, тироглобулин, у-глобу-лин человека, сывороточный альбумин, а - и р-лактоглобулин обладают существенно различными скоростями перемещения на колонке из агара. Стандартизация метода гельфильтрации позволяет его использовать не только для фракционирования белков, но и для определения молекулярного веса в весьма простом хроматографическом эксперименте. [49]
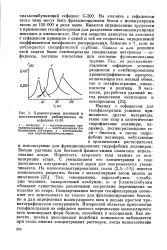 |
Хроматограмма нативной и. [50] |
Пористость агарового геля зависит от концентрации агара. С уменьшением его концентрации в геле доступность внутренних частей зерен для макромолекул увеличивается. Так, гемоцианины, тироглобулин, у-глобу-лин человека, сывороточный альбумин, а - и [ 3-лактоглобулин обладают существенно различными скоростями перемещения на колонке из агара. Стандартизация метода гельфильтрации позволяет его использовать не только для фракционирования белков, но и для определения молекулярного веса в весьма простом хроматографическом эксперименте. [51]
Миграция белков в слое агарового геля подобна их движению при свободном электрофорезе. Однако в агаровом геле значительно сильнее, чем при электрофорезе на бумаге, выражен электроосмос, который усиливает поток буферного раствора в сторону катода. Чтобы устранить возможные артефакты, следует размещать лунки для внесения исследуемого образца точно в центре агаровой пластинки. [52]
В подготовленные чашки Петри наливают расплавленный в физиологическом растворе 1 % - ный агар, содержащий 0 1 % мертио-лата, таким образом, чтобы получился слой толщиной 3 - 4 мм. В приготовленном слое агарового геля делают лунки для внесения исследуемых образцов. [53]
В сыворотке крови здорового человека при электрофорезе на бумаге можно обнаружить 5 фракций: альбумины, аг, cq -, 3 -, у-гл булины. Методом электрофореза в агаровом геле в сыворотке крови выделяют 7 - 8 фракций, а при электрофорезе в крахмальном или полиакриламидном геле-до 16 - 17 фракций. Следует помнить, что терминология белковых фракций, получаемых при различных видах электрофореза, еще окончательно не установилась. При изменении условий электрофореза, а также при электрофорезе в различных средах ( например, в крахмальном или полиакриламидном геле) скорость миграции и, следовательно, порядок белковых зон могут меняться. [54]
Реакцию проводят в пробирках, внутреннюю поверхность которых, как и в предыдущем методе, обрабатывают 0 1 % - ным раствором агара. На дно пробирки заливают агаровый гель, содержащий антисыворотку, затем последовательно наслаивают теплый раствор чистого агара и раствор АГ так, чтобы все три слоя были равной высоты - 10 - 15 мм. Пробирки герметически закупоривают и помещают в термостат. [55]
Страницы: 1 2 3 4