Крахмальный гель
Cтраница 1
Крахмальные гели подвергаются окислению, и их труднее получить свободными от ионизованных групп. Гели, синтезированные из fi - оксипропилового эфира декстрана и ЭХГ, набухают в воде и этиловом спирте. [1]
Толщина слоя крахмального геля не должна превышать 5 - 10 мм. В более толстом слое геля миграция белков происходит неравномерно. [2]
Механическая прочность крахмального геля достаточно велика, чтобы после окончания опыта его можно было целиком извлечь из прибора и окрасить зоны обычными методами, применяемыми при электрофорезе на бумаге. Обычно гель разрезается вдоль и свежая поверхность окрашивается. Если интенсивность окраски поверхности недостаточна, гель можно прокрасить по всей глубине, продержав его в красителе достаточно долго. [3]
Пластифицированный слой крахмального геля погружают на 2 ч в реактив. Избыток красителя смывают 5 % - ной уксусной кислотой, пока промывная жидкость не станет бесцветной. При последней промывке, как указано в работе [277], к уксусной кислоте добавляют 50 % глицина. [4]
Электрофорез в крахмальном геле имеет не только большое значение при диагностике парапротеинемий: он весьма важен при определении гомогенности нативных белков и полезен при анализе субъединичной структуры молекулы белка. Например, папаиновые фрагменты IgG ( Fab, Fc и Fc) или выделенные из него полипептидные цепи ( Н - и L-цепи) при электрофорезе в крахмальном геле образуют отдельные зоны. Это позволяет сравнивать субъединицы гомогенных IgQ ( миеломных белков или чистых антител) между собой. [5]
Метод Смитиса с крахмальным гелем остается чрезвычайно мощным аналитическим приемом. На каждой стадии его развития получали какие-нибудь удивительные результаты, и понятно, что многие опытные исследователи сдержанно высказываются о достоверности основанных на этих результатах заключений. Истинный механизм процесса еще не раскрыт, однако имеющиеся экспериментальные данные как будто подтверждают гипотезу о том, что при разделении имеет значение величина частиц. Например, было показано, что некоторые белки, имеющие равные подвижности при электрофорезе на бумаге, в крахмальном геле движутся со скоростями, убывающими в порядке возрастания молекулярных весов. Описаны многочисленные примеры применения электрофореза в крахмальном геле при фракционировании ферментов. Вместо прокрашивания белков красителями ферменты в зонах геля обнаруживают путем обработки геля соответствующими субстратами. [6]
 |
Иммуноэлектрофореграмма белков сыворотки крови человека ( по Генри. [7] |
При электрофорезе в крахмальном геле фракция альбуминов у некоторых людей иногда делится на две ( альбумин А и альбумин В), т.е. у таких людей имеется два независимых генетических локуса, контролирующих синтез альбуминов. Добавочная фракция ( альбумин В) отличается от обычного сывороточного альбумина тем, что молекулы этого белка содержат два остатка дикарбоновых аминокислот или более, замещающих в полипептидной цепи обычного альбумина остатки тирозина или цистеина. Наследование полиморфизма альбуминов происходит по аутосомному кодоминантному типу и наблюдается в нескольких поколениях. [8]
Закончив электрофорез, ванну с крахмальным гелем извлекают из прибора и располагают горизонтально на столе. Пленку парафина, закрывающую гель, удаляют, и всю поверхность крахмала покрывают листом фильтровальной бумаги. Лист плотно прижимают к поверхности геля в течение 5 мин, затем снимают его, высушивают в сушильном шкафу при 100 С и окрашивают белковыми красителями ( см. стр. [9]
Описанные выше методы электрофореза в крахмальном геле позволяют одновременно анализировать несколько белковых растворов ( например, сразу несколько сывороток), если использовать более широкую ванну для геля. Например, в ванне шириной 124 мм можно одновременно параллельно фракционировать 8 - 10 сывороток. [10]
Фракции белка, разделившиеся в крахмальном геле, можно идентифицировать в реакции преципитации со специфической антисывороткой. Для этого Шерлен и Голь [25] предложили комбинировать электрофорез в крахмальном геле с иммунодиффузией в агаровом геле. [11]
Белки, выделенные электрофорезом на крахмальном геле, могут содержать в качестве примеси крахмал. В этом случае, поскольку молекулярный вес обоих полимеров одного порядка, следует очень тщательно подобрать носитель. При выделении некоторых соединений из растений ферментативные реакции, ускоряющиеся после разрушения клеточных мембран, зачастую сильно снижают выход конечного продукта. [12]
Повышенная разрешающая способность электрофореза в крахмальном геле позволяет делить смесь белков на еще большее число компонентов. [13]
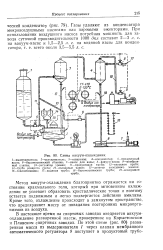 |
Схема вакуум-охлаждения. [14] |
Метод вакуум-охлаждения благоприятно отражается на состоянии крахмального геля, который при мгновенном охлаждении не успевает образовать кристаллические точки и поэтому остается подвижным и легко подвергается действию амилазы. Кроме того, охлаждение происходит в замкнутом пространстве, что предохраняет массу от попадания посторонних микроорганизмов из воздуха. [15]
Страницы: 1 2 3 4