Алюмосиликатный гель
Cтраница 4
Данные образца I относятся к так называемому напряженному образцу, т.е. образцу алюмосиликатного ксе-рогеля с цеолитом, введенным в раствором жидкого стекла на стадии сливания растворов. Для образца 2 приведены данные механической смеси порошка алюмосиликатного геля и цеолита и для порошка образца 3, полученного тщательным разрушением напряженного образца. Из табл. 9 видно, что межплоскостные расстояния кристаллов / VaA в напряженном образце уменьшены приблизительно на 0 6 % по сравнению с соответствующим параметром для кристаллов цеолита в механической смеси, что указывает на сжатие наполнителя. Исчезновение сдвига интерференционных линий после разрушения образца означает, что деформации в кристаллах цеолита имеют упругий характер. Эти опыты подтверждают реальность существования в наполненных алюмосиликатных катализаторах остаточных внутренних напряжений, и в то же время позволяют по величине г относительной деформации оценить их величину, которая, как показывает приближенный расчет, достигает нескольких десятков кг / см, т.е. находится на уровне прочности этих структур. [46]
 |
Схема получения цеолитов из гидрогелей. [47] |
В промышленных и полупромышленных условиях обычно получают натриевые формы цеолитов, а затем, в случае необходимости, путем катионного обмена с растворами соответствующих солей переводят их в другие ионообменные формы ( калиевую, кальциевую и пр. Большая подвижность катиона натрия благоприятствует более быстрой кристаллизации алюмосиликатных гелей. [48]
Интересно проследить за влиянием температуры кристаллизации на цеолитную фазу. На рис. 4.20 показана зависимость длительности кристаллизации цеолита X из алюмосиликатных гелей от температуры. [49]
Значения х, немного отличающиеся от двух в меньшую сторону, как, например, х 1 87 ( у 0 935), находятся в некотором противоречии с правилом Левенштейна, являющимся обобщением многочисленных экспериментальных данных для природных алюмосиликатов. Нам кажется, что такие небольшие отклонения от правила Левенштейна возможны для образцов цеолитов типа А, образующихся в условиях быстро протекающей кристаллизации алюмосиликатных гелей ( от 2 до 20 - 30 час. [50]
Лабораторными опытами было установлено, а промысловыми испытаниями подтверждено, что ПАСР может применяться засолоненным до насыщения NaCl, а также содержать значительное количество солей калия, кальция и магния, сохраняя при этом удовлетворительные технологические показатели. При этом необходимо учитывать, что ввод NaCl уменьшает СНС раствора и при низких значениях рН ( менее 7 5) может вызвать коагуляцию алюмосиликатного геля. [51]
Большинство значительных спектральных изменений обнаружено для молекул-индикаторов, которые, судя по экспериментальным данным, сильно взаимодействуют с активными адсорбентами, относящимися к группе алюмосиликатных гелей. Это взаимодействие является либо кислотно-основным, либо окислительно-восстановительным. [52]
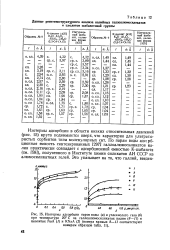 |
Изотермы адсорбции паров воды ( а и углекислого газа ( б. [53] |
Изотермы адсорбции в области низких относительных давлений ( рис. 15) круто поднимаются вверх, что характерно для ультрапористых сорбентов типа молекулярных сит. По парам воды адссрб-ционная емкость синтезированных [297] галлоалюмосиликатов калия практически совпадает с адсорбционной емкостью К-шабазита ( см. [58]), полученного в Институте химии силикатов АН СССР из алюмосиликатных гелей. [54]
Алюмосиликатный гидрогель обычно получают соосажде-нием обоих компонентов или осаждением гидрогеля окиси алюминия в присутствии свежеприготовленного гидрогеля двуокиси кремния. Морфология алюмосиликатных гелей весьма сходна с морфологией силикагелей, и, как показывают рентгенографические данные, вещество аморфно, если температура нагревания не превышает 1070 К. Как правило, первичные сферические частицы имеют средний диаметр 3 - 5 нм и такой же средний размер пор. Удельная поверхность колеблется в интервале 200 - 700 м2 / г. Содержание окиси алюминия в промышленных образцах составляет 10 - 30 мол. Характер распределения алюминия в структуре геля зависит от условий получения; в ряде случаев наблюдалось в основном равномерное распределение [112-114], что, вероятно, является типичным. Вообще соосаждение дает более равномерное распределение компонентов. [55]
Показатели ионной адсорбции алюмосиликатных гелей были исследованы Планком [20] путем сравнения кремнеземо-глинозем-ных гелей с кремнеземными и глиноземными гелями отдельно. Адсорбция катионов на кремнеземном геле может рассматриваться только как вторичная адсорбция, так как поверхность должна первоначально поглотить ион гидроксила, для того чтобы обеспечить анионные участки для адсорбции катионов. В случае алюмосиликатных гелей такие участки уже обеспечены наличием ионов алюминия в тетраэдрической координации в кремнекислородной структуре. В этих условиях адсорбция катионов происходит не только при рН выше 7, но также и в нейтральной и слабокислой среде. Планк [20] сообщает, что кремнеземо-глиноземные гели показывают свойства многоосновной кислоты, в которой кислотные участки по силе кислотности изменяются в очень широких пределах. Адсорбционная способность глиноземо-кремнеземного геля для ионов аммония быстро возрастает с увеличением ионной силы раствора, обнаруживая увеличение ионизации на слабокислотных участках катализатора. [56]
В первый период реакции содержание Si02 и А1203 в растворе возрастает и достигает максимума через 100 - 240 мин в зависимости от концентрации щелочи и температуры. В этот период образуется аморфный алюмосиликатный гель, затем гель переходит в кристаллический алюмосиликат и одновременно с этим процессом наблюдается уменьшение концентрации Si02 и А1203 в растворе. [57]
С практической стороны ионообменник должен быть химически стоек, обладать высокой обменной емкостью на единицу объема и обеспечивать большую скорость обмена. Впервые ионообменный процесс применен для умягчения воды Гансом в 1907 г.; использовались природные зеленые пески, содержащие минерал глауконит. Позднее было отдано предпочтение искусственным алюмосиликатным гелям благодаря их большей емкости. Эти материалы вполне пригодны для умягчения нейтральных вод, но возможности их применения ограничиваются неустойчивостью в разбавленных кислотах и щелочах. [58]
Однако некоторые Na-цеолиты ( например, Na-мор-денит [108]) не могут быть синтезированы из силика-алюмогелей, получаемых смешением силикатных и алю-минатных растворов. Высококремнеземный синтетический фожазит ( цеолит Na-Y) в принципе может быть получен из таких силикаалюмогелей, но кристаллизуется не воспроизводимо и не в виде чистой фазы. При применении затравок синтез цеолита Na-Y может быть легко осуществлен и из алюмосиликатных гелей. [59]
Все катализаторы этого класса имеют сильное сродство к воде. Применяется также фосфорная кислота или ее кислые соли на носителях, подобных алюмосиликатному гелю и силикагелю с окислами тантала, циркония или гафния. [60]
Страницы: 1 2 3 4