Гемоглобин
Cтраница 1
 |
Четвертичная структура. [1] |
Гемоглобин был получен из крови лошади, а миоглобин - из мышц кашалота, тем не менее эти белки имели близкое пространственное строение. [2]
Гемоглобин осуществляет перенос кислорода от легких к различным органам, в которых протекают реакции окисления. [3]
Гемоглобин является основным компонентом эритроцитов - красных кровяных клеток крови и определяет их специализированные функции - связывать и переносить кислород от легких к тканям, а углекислый газ - в обратном направлении. В одном эритроците содержится около миллиона молекул гемоглобина, общее содержание гемоглобина в крови составляет 13 - 16 г / дл. [4]
Гемоглобин раствор в 0 05 % - ном растворе хлорида натрия, концентрации 3 мг / мл. [5]
Гемоглобин количественно определяют по собственной окраске на фотоэлектроколориметре. [6]
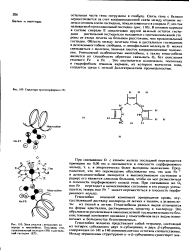 |
Структура протопорфирина IX.| Зона участка связывания кл лоро да в миоглоби не. Пока за ны гем, проксимальный гистидин ( F8 и днстальный гистидин ( Е7. [7] |
Гемоглобин основной компонент эритроцитов крови, осу-ществлвющий достааку кислорода от легких к тканям, а углекислоты из тканей в легкие. Гемоглобины разных видов отличаются по форме кристаллов, растворимости, сродстау к кислороду. Это обусловлено различиями в аминокислотной последовательности белков; гемовый компонент одинаков у гемоглобинов всех видов позвоночных и большинства беспозвоночных. [8]
Гемоглобин - дыхательный пигмент, содержащийся в эритроцитах и обусловливающий цвет крови, Представляет собой сложный белок, образованный белком глобином, связанным с гвмом. Осуществляет транспорт кислорода из легких в ткани, а из последних С02 в легкие. [9]
Гемоглобин является составной частью красных кровяных тел крови и служит в качестве переносчика кислорода от легких к тканям тела. [10]
Гемоглобин ответствен за транспорт кислорода в живом организме: I г гемоглобина связывает 1 35 см3 кислорода. Гемоглобин связывает кислород в легких и разносит его по всему организму. При связывании с гемоглобином кислород выступает как лиганд по отношению к атому железа. Токсичные свойства монооксида углерода определяются тем, что он является еще более сильным лигандом и препятствует связыванию и транспорту кислорода. [11]
Гемоглобин ( НЬ) относится к группе сложных белков хромопротеинов. Он состоит из белка глобина и просте-тической группы - тема, содержащего двухвалентное железо. В этом виде в крови содержится основная часть гемоглобина. При вдыхании угарного газа СО в крови образуется карбок-сигемоглобин НЬСО, соединение более прочное, чем оксигемоглобин, что приводит к отравлению организма. При действии на кровь окислителей двухвалентное железо гемоглобина окисляется в трехвалентное и гемоглобин превращается в метгемоглобин ( МНЬ), который, как и карбоксигемоглобин, неспособен присоединять кислород. Гемоглобин и его производные обладают способностью поглощать излучение различной длины волн и давать характерные спектры поглощения. [12]
Гемоглобин определяют по Сали в специальных пробирках ( гемометрах), превращая гемоглобин соляной кислотой в солянокислый гематин. После промывки пипетки ( несколько раз подряд-набирают соляную кислоту и выдувают ее обратно в гемометр) кровь размешивают специ - аль ной пало чкой и оставляют стоять 3 мин. После этого подгоняют цвет жидкости в гемометре к цвету шкалы ( окрашенное втекло или стандартные пробирки) путем добавления в нее по - каплям дистиллированной воды. При одинаковых цветах высота жидкости в пробирке указывает на число Сали в процентах. В настоящее время широко применяют выражение количества гемоглобина в грамм-процентах. [13]
Гемоглобин в водном растворе обратимо связывает различные растворенные газы, особенно кислород и окись углерода. [14]
Гемоглобины различных животных ведут себя не совсем одинаково. [15]
Страницы: 1 2 3 4