Гемоглобин
Cтраница 3
Гемоглобин - не единственный белок, содержащийся в организме человека, который претерпевает генетические изменения, обусловленные мутациями. Все белки, глобулярные и фибриллярные, подвержены мутациям. Гемоглобину уделяют значительно больше внимания просто потому, что многие изменения молекулярной структуры гемоглобина вызывают у людей выраженные нарушения кровообращения или дыхания. [31]
Гемоглобин же содержит четыре центра связывания, по одному в каждой из четырех субъединиц, причем все эти центры действуют кооперативно. Вспомним, что когда один центр связывания гемоглобина занят молекулой кислорода, у других центров связывания сродство к кислороду возрастает. Это проявляется в том, что после связывания первой молекулы кислорода кривая насыщения гемоглобина кислородом резко идет вверх и принимает сигмоидную форму. Аналогичным образом гомотропный аллостерический фермент ( рис. 9 - 21, А) имеет несколько центров связывания для своего субстрата, действующих кооперативно, так что связывание одной молекулы субстрата значительно облегчает присоединение к ферменту последующих молекул субстрата. Поэтому зависимость скоро -, сти ферментативной реакции от концентрации субстрата описывается сигмоидной, а не гиперболической кривой. [32]
 |
Потребление кислорода ( в относительных величинах основными органами тела человека ( взрослого мужчины. [33] |
Гемоглобин состоит из двух а - и двух р-полипептидных цепей и четырех ге-мовых групп, каждая из которых присоединена к полипептидной цепи ( разд. Одна гемовая группа обратимо связывает одну молекулу молекулярного кислорода. Поскольку гемоглобин содержится в эритроцитах в большом количестве, в 100 мл цельной крови млекопитающего при полном насыщении кислородом транспортируется приблизительно 21 мл газообразного кислорода. Связывание кислорода гемоглобином зависит от четырех факторов: 1) парциального давления О2; 2) рН - 3) концентрации 2 3-бисфосфоглицерата и 4) концентрации СО 2 ( разд. На рис. 24 - 21 приведены кривые насыщения гемоглобина кислородом. [34]
Гемоглобин представляет собой соединение белка глобина с красящим началом гемом. Вне организма гемоглобин, при действии воздуха, превращается в метгемоглобин, который отличается от оксигемоглобина прочностью связи с кислородом. [35]
Гемоглобин содержится в эритроцитах и играет большую роль в процессах дыхания: присоединяя кислород, он переходит в оксигемоглобин, который отдает присоединенный кислород тканям. [36]
Гемоглобин содержится в эритроцитах. Так как эритроциты постепенно отмирают, а на смену им синтезируются новые, то оказывается, что в течение 3 - 4 месяцев все количество гемоглобина полностью обновляется. Распад эритроцитов происходит в клетках печени, селезенки и костного мозга, при этом гемоглобин расщепляется на белок - глобин, железо и желчные пигменты: биливер-дин и билирубин. [37]
Гемоглобин играет большую роль в жизнедеятельности организма, так как выполняет в нем функции переносчика кислорода. [38]
Гемоглобин при помощи железа может присоединять не только кислород, но и окись углерода. Валентность железа при этом тоже не меняется. Ядовитое действие окиси углерода проявляется в том, что образующийся карбоксигемоглобин становится непригодным к переносу кислорода, в результате чего наступает кислородное голодание. При связывании 70 % гемоглобина окисью углерода наступает смерть. [39]
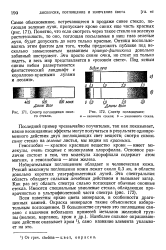 |
Спектр поглощения сине.| Спектр поглощения. а - оконного стекла. б - увнолевого стекла. [40] |
Гемоглобин - красное красящее вещество крови - имеет молекулы, очень сходные с молекулами хлорофилла. Основное различие состоит в том, что молекула хлорофилла содержит атом магния, а гемоглобина - атом железа. [41]
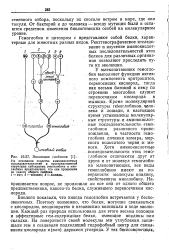 |
Эволюция глобинов. [42] |
Гемоглобин и цитохром с представляют собой белки, характерные для животных разных видов. Рентгенографическое исследование и изучение аминокислотных последовательностей этих белков для различных-организмов позволяют проследить пу ти их эволюции. [43]
Гемоглобин, содержащийся в эритроцитах, и его производные играют чрезвычайно важную роль в дыхательной функции крови - переносе газов от легких к тканям и обратно. [44]
Гемоглобин взрослых и эмбрионов отличается по растворимости и форме кристаллов. [45]
Страницы: 1 2 3 4