Каталитическая активность - металл
Cтраница 1
Каталитическая активность металлов зависит от ряда различных факторов. Их совместное действие, однако, настолько сложно, что теоретические представления в большинстве случаев позволяют объяснить только какую-либо одну сторону вопроса. Так, несомненно существующая глубокая связь между каталитическими свойствами и электронным строением металла часто заслоняется другими явлениями, связанными с катализом более косвенно. [1]
Каталитическая активность металлов в указанных процессах большей частью невысока. Практического применения в катализе металлы подгруппы хрома не имеют, и исследование их каталитических свойств обычно носит теоретический характер. [2]
Каталитическая активность металлов, входящих в ферментные системы, особенно велика. Это можно видеть, например, in сопоставления следующих данных: 1 грамм-атом Fe или Fe J - разрушает при 0 за 1 минуту в водном растворе 6 - Ю 1 моля H2OL; l моль гемнна ( при тех же условиях) разрушает 6 - Ю - моля, а I моль каталазы - 5 - Ю6 моля. [3]
Часто каталитическая активность металлов сопоставляется с наличием вакансий в d - зоне металла. [5]
Каталитическая активность металлов переменной валентности в процессах окисления и старения синтетических каучуков зависит от следующих факторов: природы металла переменной валентности; валентного состояния металла; химической структуры каучука; содержания металла переменной валентности; природы ан-тиокснданта, применяемого для стабилизации каучука; наличия в каучуке веществ, способных связывать металлы переменной валентности в соединения ( комплексы или хелаты), которые являются неактивными в процессах окисления или других превращениях каучуков. [6]
Если каталитическая активность металла или иона металла зависит от природы и расположения лигандов в кристалле, то подобное же расположение можно найти и в молекулах металлоорганических соединений, которые могут оказаться уже не гетерогенными, а гомогенными катализаторами. [7]
Так как каталитическая активность металла тем больше, чем сильнее развита его поверхность, при приготовлении катализаторов стараются по возможности ее увеличить. С этой целью металл часто осаждают на каком-либо индифферентном пористом материале, например асбесте. [8]
Так как каталитическая активность металла тем больше, чем сильнее развита его поверхность, при приготовлении катализаторов стараются по возможности ее увеличить. С этой целью металл часто осаждают на каком-либо индифферентном пористом материале, например асбесте. [9]
Так как каталитическая активность металла тем больше, чем сильнее развита его поверхность, при изготовлении катализаторов стараются по возможности ее увеличить. С этой целью металл часто осаждают на каком-нибудь индифферентном пористом материале, например асбесте. [10]
Особенно велика каталитическая активность металлов, у которых сумма d - и s - элек-тронов выше, чем число электронов, участвующих в металлической связи, так как наличие неспаренных электронов на внешних d - и s - орбиталях особо выгодно для поверхностных взаимодействий. В приближенном рассмотрении катализ на металлах основан на активированной адсорбции ( хемосорбции) реагентов поверхностью катализатора, которая сопровождается акцепторно-донорными переходами электронов в d - оболочку металла и в обратном направлении в зависимости от типа реакций. Однако этими переходами не исчерпывается вся сущность каталитического акта. [11]
Особенно велика каталитическая активность металлов, у которых сумма d - и s - электронов выше, чем число электронов, участвующих в металлической связи, так как наличие неспаренных электронов на внешних d и s - орбиталях особо выгодно для поверхностных взаимодействий. В приближенном рассмотрении катализ на металлах основан на активированной адсорбции ( хемосорбции) реагентов поверхностью катализатора, которая сопровождается акцепторно-донорными переходами электронов в d - обо-лочку мета лла и в обратном направлении, в зависимости от типа реакций. Однако нельзя считать, что этими переходами исчерпывается вся сущность каталитического акта. [12]
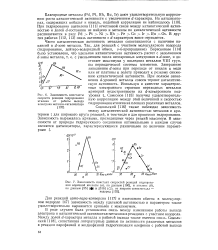
Совокупность данных каталитической активности металлов в отношении различных реакций позволяет заключить, что удельная каталитическая активность переходных металлов резко меняется в зависимости от степени заполнения rf - зоны, причем максимуму каталитической активности для разных реакций соответствует различная степень заполнения электронами cf - зоны. Основной причиной этого различия является специфичность строения и свойств активных комплексов различных реакций. Существенное влияние, кроме того, может оказывать воздействие реакционной смеси на катализатор, проявляющееся в растворении отдельных компонентов, что приводит к изменению электронной структуры, а следовательно, и свойств металлических катализаторов. [13]
В отношении каталитической активности металлов в обмене углеводородов можно отметить следующее. [14]
Сокольский сопоставил каталитическую активность металлов в реакциях с уча стием водорода с их положением в периодической системе. [15]
Страницы: 1 2 3 4