Геометрия
Cтраница 2
Геометрия может основываться и на таких элементах, как прямые, плоскости, окружности, сферы. [16]
Геометрия еще в XIX веке, кроме единственного, приобрела множественное число, и любая пз чистых геометрий накопила в XX веке большое количество результатов, заслуживающих отдельных обзоров. Так, например, возникла кв атернпонная проективная геометрия. Пример развития в другом направлении дает нам история той же проективной геометрии: создание проективно-дифферен-циальной геометрии. Наряду с такими общими концепциями и построениями было решено много важных задач в более конкретной постановке, например в алгебраической геометрии. [17]
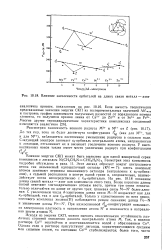 |
Влияние заселенности орбиталей на длину связи металл - азот. [18] |
Геометрия этих комплексов подробно обсуждена в разд. Этот лиганд образует вокруг центрального атома так называемый одношапочный октаэдр ( КЧ 7): шесть донорных атомов занимают вершины искаженного октаэдра ( направлены к ег-орбита-лям), а седьмой расположен в центре одной грани и, следовательно, взаимодействует почти непосредственно с 2г - орбиталью. На рис. 10.18 показаны длины связей металл - азот для комплексов этого типа. Более короткие длины связей отвечают октаэдрическим атомам азота, причем три связи незначительно отличаются по длине от других трех; граневая связь М - N более длинная. С увеличением числа d - электронов длина связи М - N возрастает как для ег-орбиталей, так и для g - орбиталей. [19]
Геометрия применяемых при этом резцов выбирается в зависимости от вида и свойств обрабатываемого материала и материала резца. Для обработки пластмассы, эбонита, твердой резины алмазные резцы снабжаются одной радиусной режущей кромкой. [20]
Геометрия другого структурно изученного карбонильного комплекса рутения - бис - ( дибромо-рутений-трикарбонила) [ RuBr2 ( CO) 3 ] 2 [138], близка к найденной для [ ВгМгЦСОЬЬ [99]: группы Ru ( CO) 3Br объединены в димерную молекулу посредством мостиковых атомов брома ( рис. 21в), так что октаэдры сочленяются по общему ребру. Длины мостиковых и концевых связей Ru-Вг 2 571 и 2 543 А различаются мало, экваториальные связи Ru-С ( 1 90 А) короче аксиальной ( 1 97 А), С-Оэкв. [21]
Геометрия и свойства фрагментов гомодиметаллических карбонильных л-комплексов переходных металлов подробно рассмотрены ранее, укажем только на их основную особенность: атом переходного металла М содержит неспаренный электрон, способный участвовать в а-связи с атомом непереходного элемента группы IVB, а также несвязывающие nd - электроны, которые могут быть использованы для образования л-связей с участием р я - или d л - орбит атомов лигандов. [22]
Геометрия одной из структур типа цинковой обманки кратко упоминалась уже на стр. Структура такого типа выводится из структуры алмаза заменой половины атомов углерода на атомы А, а другой половины - на атомы В, причем эта замена должна обеспечить взаимную тетраэдрическую координацию частиц обоего сорта. Подобная замена ведет к снижению симметрии, что, например, соответствует переходу от класса m3m к классу 43т; запись кристаллохимической формулы приобретает вид AWBW кб. Со структурой цинковой обманки тесно связан другой тип кристаллических соединений типа АВ, опять с взаимной тетраэдрической координацией обоих сортов атомов, обладающий, однако, не кубической, а гексагональной симметрией. Этот структурный тип называется вюртцитовым по гексагональной модификации ZnS - вюртциту. Ему соответствует кристаллохимическая формула А 4Ш [4] гк. Соотноше - ния между вюртцитом и цинковой обманкой аналогичны соотношениям между гексагональной и кубической плотнейшими упаковками. В табл. 21 приведены некоторые представители обоих структурных типов сульфида цинка. Характер химической связи у этих соединений лежит в широком интервале между чисто ионной и чисто ковалентной связями ( ср. [23]
Геометрия этой частицы подобна геометрии промежуточных соединений, возникающих при перегруппировках в ионах карбония, однако в случае радикала между тремя атомами углерода должны быть распределены три. Это положение аналогично обсужденному в дополнении 1, где было показано, что ци-клопропенильный катион, в котором два п-электрона распределены между тремя атомами углерода, значительно более устойчив, чем циклопропенильный радикал с тремя я-электронами. Расчеты энергии промежуточных соединений при ионных и радикальных перегруппировках по методу молекулярных орбиталей также показывают, что случай с тремя электронами гораздо менее выгоден. Однако миграция фенильного радикала может сопровождаться образованием мости-кового радикала, для которого нет необходимости предполагать неклассическое строение. [24]
Геометрия по своему происхождению является наукой опытной. Из всех мыслимых геометрий только опыт может выбрать ту, которая описывает правильно соотношения геометрических объектов реального мира. Правая система прямоугольных декартовых координат никакими движениями в пространстве не может быть совмещена с левой. [25]
Геометрия занимается изучением объектов, которые могут быть в том или ином смысле отождествлены с точками, и представляет собой математическую модель, воспроизводящую отношения между этими объектами. [26]
Геометрия на плоскости, которую мы изучаем в школе, основанная на немногих идеальных гладких, симметричных формах. [27]
 |
Поверхность образца кремния после проведения послойного анализа.| Профилограмма поверхности кремниевой - толщина удаленного слоя. hi - высота выступов, окружающих область сканирования. [28] |
Геометрия и объем отдельных кратеров в течение анализа поддерживаются постоянными, так как энергия, выделяющаяся в момент пробоя вакуумного промежутка, определяется величиной межэлектродного зазора, который во время эксперимента остается неизменным. [29]
Геометрия одного раствора циркуля должна быть поэтому понимаема только в том смысле, что допускается и проведение прямых линий, причем делают построения возможно более простыми. [30]
Страницы: 1 2 3 4