Двухвалентный германий
Cтраница 1
Двухвалентный германий в солянокислом растворе легко восстанавливается на капающем ртутном катоде до металла, давая хорошо выраженный диффузионный ток. [1]
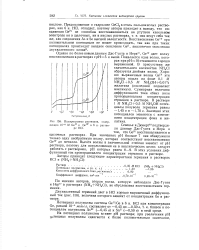 |
Подпрограмма растворов, содержащих 10 4 М Ge11 и GeIV в 6 н. растворе НС1. [2] |
Двухвалентный германий дает в НС1 хорошо выраженный диффузионный ток ( рис. 158), величина которого зависит от концентрации Ge в растворе. [3]
Сульфид двухвалентного германия, так же как и сульфид двухвалентного олова, растворяется только - в многосернистом ( желтом) аммонии в результате окисления его до четырехвалентного. [4]
Соединения двухвалентного германия - сильные восстановители; они легко окисляются в соединения четырехвалентного германия. [5]
Соединения двухвалентного германия малоустойчивы и легко разлагаются. Они являются сильными восстановителями. Наиболее характерны соединения четырехвалентного германия. [6]
Соединения двухвалентного германия мало устойчивы, обладают четко выраженными восстановительными свойствами и склонны к переходу в более устойчивые соединения высшей валентности. [7]
Соединения двухвалентного германия мало устойчивы, являются сильными восстановителями, легко окисляются на воздухе и склонны к диспро-порционированию на четырехвалентный и элементарный германий. [8]
Гидроокись двухвалентного германия может быть получена восстановлением фосфорноватистой кислотой раствора ОеОа в крепкой НС1 с последующим осаждением избытком аммиака. Все операции проводятся в атмосфере азота. Выделяется Ge ( OH) s в виде рыхлого осадка, цвет которого ( белый, желтый или красный) зависит от условий получения. [9]
 |
Проекции структур InS ( a, GeS ( б ( слои перпендикулярны плоскости рисунка. Штриховые линии - связи In - In ( а. [10] |
Соединения двухвалентного германия хорошо известны. Доказательства того, что фаза GeO стабильна при температурах ЮОО К ( ср. [11]
Гидроокись двухвалентного германия может быть получена восстановлением фосфорноватистой кислотой раствора Qe02 в крепкий НС1 с последующим осаждением избытком аммиака. Все операции проводятся в атмосфере азота. Выделяется Qe ( OH) 2 в виде рыхлого осадка, цвет которого ( белый, желтый или красный) зависит от условий получения. [12]
Известен нитрид двухвалентного германия GesN2, отличающийся меньшей химической стойкостью. [13]
Восстановительные свойства двухвалентного германия проявляются сильнее в щелочной среде и, следовательно, окисление двухвалентного германия до четырехвалентного протекает легче в щелочной, нежели в кислой среде. [14]
Известны соединения четырехвалентного и двухвалентного германия. Первые из них более устойчивы. Ниже рассмотрены некоторые, наиболее важные для технологии, химические соединения германия. [15]
Страницы: 1 2 3 4