Двухвалентный германий
Cтраница 3
Растворяясь в сильных кислотах, Ge ( OH) 2 дает соли двухвалентного германия. [31]
Из работы В. А. Назаренко по химии германия [141] известно, что простые некомплексные ионы двухвалентного германия в водных растворах не существуют, в то время как соединения 4-валентного германия в водных растворах более устойчивы. В водных растворах 4-валентный германий может находиться в виде разнообразных ионов. [32]
Германий в земной коре в основном содержится в виде четырехвалентного, так как соединения двухвалентного германия могут образовываться только в сильно восстановительной среде. По сравнению с двуокисью кремния и силикатами, двуокись германия и соответствующие германаты гораздо больше растворимы в воде и слабокислых растворах, так что из твердых растворов германатов в силикатах или двуокиси германия в двуокиси кремния германий вымывается в большей степени, чем кремний, поэтому весьма редко отмечается резко повышенное содержание его в силикатах. Двуокись германия, германаты и алюмогерманаты плавятся при более низкой температуре, чем двуокись кремния и соответствующие силикаты и алюмосиликаты, следовательно, при остывании магмы германий должен был сопутствовать соединениям, кристаллизующимся при низких температурах. Этим, по-видимому, и объясняется, например, обогащение германием гранитов по сравнению с нефелинсиенитовы-ми пегматитами. [33]
Восстановительные свойства двухвалентного германия проявляются сильнее в щелочной среде и, следовательно, окисление двухвалентного германия до четырехвалентного протекает легче в щелочной, нежели в кислой среде. [34]
Германий в земной коре в основном содержится в виде четырехвалентного, так как соединения двухвалентного германия могут образовываться только в сильно восстановительной среде. По сравнению с двуокисью кремния и силикатами, двуокись германия и соответствующие германаты гораздо больше растворимы в воде и слабокислых растворах, так что из твердых растворов германатов в силикатах или двуокиси германия в двуокиси кремния германий вымывается в большей степени, чем кремний, поэтому весьма редко отмечается резко повышенное содержание его в силикатах. Двуокись германия, германаты и алюмогерманаты плавятся при более низкой температуре, чем двуокись кремния и соответствующие силикаты и алюмосиликаты, следовательно, при остывании магмы германий должен был сопутствовать соединениям, кристаллизующимся при низких температурах. Этим, по-видимому, и объясняется, например, обогащение германием гранитов по сравнению с нефелинсиенитовы-ми пегматитами. [35]
При нагревании в гипофосфористой кислоте Ge02 растворяется, образуя желто-зеленый раствор, дгюдий реакции на двухвалентный германий ( см. стр. [36]
Таким образом, легкость диссоциации с образованием GeClz и восстановительная способность характеризуют GeHCl3 как производное двухвалентного германия. [37]
Таким образом, легкость диссоциации с образованием GeCl2 и восстановительная способность характеризуют GeHCl3 как производное двухвалентного германия. [38]
Необходимо, чтобы концентрация кислоты была не ниже указанной, в противном случае может произойти осаждение сульфида двухвалентного германия. Образование оранжевого осадка при отстаивании свидетельствует не о незавершенном восстановлении, а о частичном окислении вещества в растворе под действием кислорода воздуха. [39]
Он возгоняется в виде белого гигроскопического порошка, который легко растворяется в воде, образуя раствор фторида двухвалентного германия, обладающий характерными восстановительными свойствами. Из подкисленного раствора GeF2 сероводород осаждает сульфид германия. [40]
Помимо описанного выше, для Ge ( и Sn) известен нитрид состава Ge3N2, являющийся производным двухвалентного германия. Он представляет собой темно-коричневый порошок, легко подвергающийся гидролизу. Распад Ge3N2 на элементы начинается около 500 С. [41]
Легкая превращаемость соединений двухвалентного германия в соединения четырехвалентного германия позволяет предполагать, что GeJ2 - наиболее доступный галогенид двухвалентного германия, должен алкили-роваться диарилртутью с образованием германийорганических соединений. Известно [1], что GeJ2 присоединяет RJ с образованием RGeJ3 - При взаимодействии GeJ2 с ( C2H5) 2Hg и ( re - C4H9) 2Hg [2] выделяется металлическая ртуть. [42]
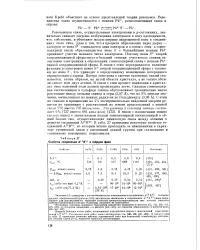 |
Свойства соединений AIVBVI в твердой фазе. [43] |
Согласно модели, предложенной Кребсом [418], валентность катионов в соединениях A Vyj VI равна двум Однако для двухвалентного германия значений электроотрицательности нет, поэтому разность электроотрицательностей для теллурида германия не приводится. [44]
Раствор восстановленной соли германия охлаждают льдом и нейтрализуют концентрированным водным раствором аммиака ( 50 - 60 мл), пока не появится устойчивый осадок гидрата окиси двухвалентного германия, окрашенный в кремовый цвет. Красно-коричневый осадок отделяют на воронке Бюхнера и промывают дестиллированной водой, слегка подкисленной соляной кислотой. Если препарат не должен быть использован немедленно, его высушивают в вакууме над фосфорным ангидридом. [45]
Страницы: 1 2 3 4