Элементарный германий
Cтраница 1
Элементарный германий, так же как и кремний, представляет собой полимер со структурой алмаза. Расаоложенный в периодической системе элементов рядом с кремнием, германий обладает одинаковым с ним электронным строением и свойствами. [1]
Элементарный германий, полученный из GeO2 после самой тщательной химической очистки, содержит следы примесей, которые делают его непригодным для использования в качестве полупроводника. Дальнейшую очистку германия производят кристаллофизическими методами, в основе которых лежит распределение примесей между кристаллами и расплавом очищаемого вещества. [2]
Элементарный германий и его окисные соединения не токсичны. Однако в виде пыли они вызывают раздражение дыхательных путей. Тетрахлорид германия под действием влажного воздуха выделяет токсичный дым. Токсическими свойствами обладают германоводороды. [3]
Элементарный германий химически довольно сильно отличается от металлов, со всеми галогенами германий взаимодействует с образованием тетрагалидов ковалентной природы. На воздухе при обычной температуре германий вполне устойчив, с кислородом реагирует лишь выше 700 С. Германий легко взаимодействует с серой, но с азотом непосредственно не соединяется. Вода и разбавленные кислоты при обычной температуре не действуют на германий. Концентрированные азотная и серная кислоты окисляют германий, сами восстанавливаясь при этом до диоксидов азота и серы. Германий не взаимодействует с растворами чистых щелочей, но легко реагирует с щелочными растворами пероксида водорода. Получение германия в чистейшем виде имеет крайне важное значение, но представляет большие трудности, так как германий является очень редким и сильно рассеянным элементом. [4]
Элементарный германий имеет светло-серый цвет, уд. Германий очень хрупок, легко разбивается на куски и может быть растерт в тонкий порошок. [5]
Элементарный германий имеет структуру алмаза ( рис. Х-6) с ядерным расстоянием d ( GeGe) 2 45 А. Энергия связи Ge-Ge в металле равна 45 ккал / моль. Выше 550 С германий становится пластичным и поддается механической обработке. Как и у висмута ( рис. 1Х - 43), по мере повышения давления температура плавления германия последовательно снижается и при 180 тыс. от становится равной 347 С. [6]
Элементарный германий и его окисные соединения не токсичны. Однако в виде пыли они вызывают раздражение дыхательных путей. Тетрахлорид германия под действием влажного воздуха выделяет токсичный дым. Токсическими свойствами обладают германоводороды. [7]
Из элементарного германия изготавливают линзы для приборов инфракрасной оптики ( германий прозрачен для инфракрасных лучей), дозиметры ядерных частиц, анализаторы в рентгеновской спектроскопии. [8]
При регенерации отходов элементарного германия чаще пользуются прямым хлорированием при температуре порядка 400 С. [9]
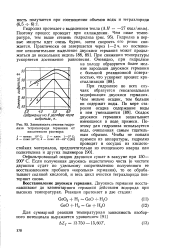 |
Зависимость степени гидролиза тетрахлорида германия от кислотности раствора. [10] |
Двуокись германия восстанавливают до элементарного германия действием водорода при высоких температурах. [11]
Облучению дейтронами или протонами подвергают элементарный германий, который затем растворяют в царской водке. Азотную кислоту удаляют упариванием с НС1, затем отгоняют Четыреххлористый германий. Оставшийся в растворе 74As переводят из Asv в As111 бромистоводородной кислотой и затем 74AsCb отгоняют. [12]
В стеклах, обогащенных германием, элементарный германий, в отличие от мышьяка, выделяется, по-видимому, в мелкодисперсном кристаллическом состоянии. Об этом свидетельствует непрозрачность, стекол составов № 38 - 41 в ИК-области, невозможность определения границы пропускания света у стекол этих составов. Следовательно, относительно хорошая проводимость структурных образований германия и мышьяка подавляется, блокируется основной стеклообразной сеткой GeSe4 / 2, лимитирующей перенос носителей тока. [13]
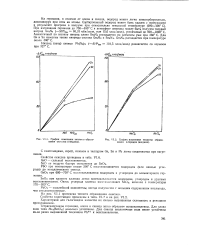 |
График изменения теплоты образования окислов ( твердых.| График изменения теплоты образования хлоридов ( жидких. [14] |
С восстанавливается водородом и углеродом до элементарного германия. [15]
Страницы: 1 2 3 4