Герцфельд
Cтраница 3
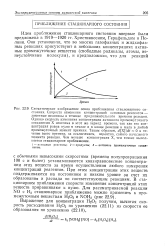
Однако, как показали Раис и Герцфельд [1063], вследствие двоякого действия стенок, возможны такие случаи, когда, несмотря на наличие гетерогенных стадий реакции, ее скорость не будет зависеть от величины 5: V. Таким образом, мы должны заключить, что рассматриваемый метод дает однозначное указание о влиянии гетерогенного фактора на течение реакции лишь в тех случаях, когда скорость реакции оказывается зависящей от величины отношения поверхности стенок реакционного сосуда к его объему. При независимости скорости реакции от величины 5: У; заключение о том, что реакция на всех ее стадиях протекает р гомогенной ( газовой) фазе, не всегда может быть правильным, и следовательно, решение вопроса о влиянии гетерогенного фактора на реакцию требует дополнительного исследования. [31]
Математическая теория цепных реакций была развита Герцфельдом ( 1921), Христиансеном с Крамерсом ( 1923), Бурсианом с Сорокиным ( 1931) и особенно в ряде работ Семенова, начиная с 1927 г. Полная теория довольно сложна. В самом элементарном виде она заключается в следующем. [32]
Такой критерий, как отмечают Раис и Герцфельд [15], может быть обманчивым и может лишь означать, что скорость реакции ( возможно, и гетерогенной) не зависит от отношения поверхности к объему. Подобный случай встречается в цепных реакциях, когда цепи как зарождаются, так и гибнут на стенках. [33]
Такой критерий, как отмечают Райе и Герцфельд [15], может быть обманчивым и может лить означать, что скорость реакции ( позможпо, и гетерогенной) не зависит от отношения поверхности к объему. Подобный случай встречается в цепных реакциях, когда цепи как зарождаются, так и гибнут иа стенках. [34]
На основании предложенного механизма крекинга этана Раис и Герцфельд вычислили, что кинетический порядок суммарной реакции крекинга этана должен быть первым, а энергия активации должна равняться 73 Кал, что хорошо совпадает с экспериментальными данными. [35]
Основываясь на термодинамике смешанных фаз, Ван-Лаар, Герцфельд и Гейтлер и Гильдебранд создали довольно стройную термодинамическую теорию жи цких растворов или, вернее, жидких смесей, охватывающую ряд их свойств: давление и состав пара, растворимость, температуры замерзания и кипения, теплоты образования и другие. [36]
Если принять, как это и делают Франк и Герцфельд, что коэффициент поглощения будет одним и тем же, независимо от того, связан ли хлорофилл с АС02 или с любым из семи промежуточных продуктов ( см. схему на фиг. VII), то при стационарном состоянии количество [ АСО2 ] и семи промежуточных продуктов должно быть тем же самым. [37]
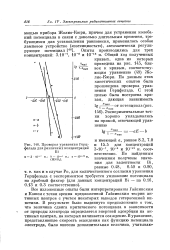 |
Проверка уравнения Герцфельда для различных концентраций Bi. [38] |
По данным этих кинетических опытов была произведена проверка уравнения Герцфельда. [39]
Решение этого вопроса было независимо предложено Христиансеном [3], Герцфельдом [4] и Полдни [5] примерно в одно и то же время. [40]
Предположение о существовании стабильного соединения АСО2 было использовано Франком и Герцфельдом [98] в их подробной теории фотосинтеза - теории, наиболее разработанной из всех имеющихся в литературе. Довольно сложный химический механизм, на котором был основан их кинетический анализ, представлен в томе I схемой на фиг. [41]
Пожалуй, наиболее современное изложение этих вопросов можно найти в обзоре Герцфельда и Мейера [38], в которой имеется глава, специально посвященная теории групп и кристаллическому полю. В этой книге приводится довольно полная библиография по этой теме. [42]
Термическое расщепление насыщенных углеводородов происходит по радикально-цепному механизму, предложенному Раисами и Герцфельдом. [43]
Оптический метод для изучения адсорбированного слоя был недавно вновь применен Фрэзером [41] по предложению Герцфельда. [44]
Страницы: 1 2 3 4