Гетеролиз - связь
Cтраница 2
По-видимому, несколько промежуточное положение по скорости гетеролиза связи С-X в карбанионе I занимает 302С6Н6 - группа. Изучение реакции цис - и тораме-фенил-р-фенилсульфонилвинилкетонов с N3 - - ионом показало, что наряду с основным продуктом торакс-фенил-р-азн - довинилкетоном образуется небольшое количество ( 3 - 6 %) 5-фенилизо-ксазола. Если при этом не имеет место смена механизма, то следует полагать, что нуклеофильное замещение для пары транс-цис - CeH5COGH CHS02C6H5 не идет стереоспецифически, так как из обоих исходных изомеров получен в основном тракс-изомер. [16]
В заключение рассмотрим реакции, в которых происходит гетеролиз связи С-С, т.е. уходящей группой является органическая молекула. Как указывалось в разделе 20.1, такие реакции называются анионным расщеплением и часто происходят по механизму S l с промежуточным образованием карбаниона. Следовательно, повышение стабильности карбаниона облегчает реакцию. В подавляющем большинстве случаев промежуточно образующийся карбанион реагирует с донором протона, присутствующим в растворе, и конечным продуктом является соответствующая СН-кислота. Реакции анионного расщепления делятся на две группы. К первой группе относятся процессы расщепления, ведущие к отщеплению карбонильных соединений в качестве уходящей группы. [17]
Высказано предположение [26], что в рассматриваемых превращениях гетеролиз связи С - Н может быть сопряжен с присоединением отщепляющегося протона к реаленту, если он еще не несет положительного заряда. [18]
Катализаторы, очевидно, влияют только на первой стадии гетеролиза связи - С-ОН. [19]
Таким образом катион типа С, образующийся в результате гетеролиза связи С - X, может превращаться в. [20]
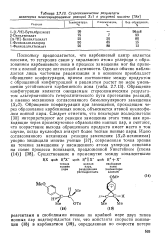 |
Стереохимические результаты некоторых неассоциированных реакций S l в уксусной кислоте [ 38а ]. [21] |
Поскольку предполагается, что карбениевый центр является плоским, то гетеролиз связи у хирального атома углерода с образованием карбениевого иона в процессе замещения мог бы привести к полной потере оптической активности. Обращение конфигурации при замещении, проходящем через образование карбениевых ионов, объясняется атакой нуклеофи-лом ионной пары. Следует отметить, что некоторые исследователи [30] интерпретируют все реакции замещения этого типа как проходящие через промежуточное образование ионных пар, и считают, что возрастание выхода обращенного продукта имеет место в том случае, когда нуклеофил атакует более тесные ионные пары. [22]
Само собой разумеется, что электрофильные реагенты, которые облегчают гетеролиз связи С - X ( протонные кислоты, кислоты Льюиса), являются катализаторами аллильной перегруппировки. Заметим, что аллиль-ные соединения ионизируются значительно легче, чем соответствующие насыщенные соединения. Это является следствием значительно большей устойчивости мезо-мерных катионов по сравнению с устойчивостью простых ионов карбония ( стр. [23]
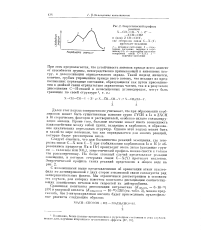 |
Энергетический профиль. [24] |
Следует отметить, что для большинства реакций замещения, где гетеролиз связи С-X или С-Y при стабилизации карбанионов 1а и 16 [ с образованием продуктов Пв и Пг ] происходит очень легко ( уходящие группы - галогены или N02), энергетический профиль можно свести к только что рассмотренному. Но более сложный случай представляют реакции замещения, в которых гетеролиз связи С - X ( Y) протекает медленно. [25]
Способность алкоксильных групп стабилизовать соседний катион ( см. раздел 4.3.6) облегчает гетеролиз связи углерод-галоген в а-галогенэфирах, в результате чего эти соединения проявляют исключительно высокую реакционную способность в условиях, способствующих реализации как 5 1 -, так и 5лг2 - механиз-мов. [26]
Способность алкоксильных групп стабилизовать соседний катион ( см. раздел 4.3.6) облегчает гетеролиз связи углерод-галоген в а-галогенэфирах, в результате чего эти соединения проявляют исключительно высокую реакционную способность в условиях, способствующих реализации как 5 у1 -, так и 5 2-механиз-мов. [27]
 |
Схема электронных состояний. о - атома фтора. б - двухвалентного фторкатиона. в - аниона фтора. [28] |
Кроме рассмотренного выше процесса поляризации связи вплоть до образования свободных ионов ( гетеролиза связи) возможен и другой процесс - разделение электронов связи с образованием свободных радикалов - гомолйз связи. Углеродный атом свободного радикала обладает тремя одинаковыми заполненными орбиталями и одной одноэлектронной орбиталыо. Таким образом, он находится в состоянии р2 - гибриди-зации. [29]
Причина этих различий в ходе реакции, по-видимому, кроется в разной скорости гетеролиза связи С-X в соответствующих карбаниояах I, образующихся при атаке нуклеофильного реагента по 3-углеродному атому соединения. [30]
Страницы: 1 2 3 4