Гибридизация - атом
Cтраница 1
 |
Односвязные ковалентные радиусы ( А. [1] |
Гибридизация атомов оказывает влияние на их ковалентные радиусы. Поскольку s - орбиталь более сжатая, чем р-орбитали, радиус уменьшается с повышением s - характера. [2]
Гибридизация атома S - sp3; связи S-О почти двойные ( см., напр. В ИК спектрах проявляются асимметрич. [3]
Поскольку гибридизация атома галогена практически постоянна, то константа квадрупольной связи будет линейной функцией степени ионности связи /, которая грубо пропорциональна разности электроотрицательностей. Так, частоты ЯКР атома хлора в хлорорганических соединениях примерно вдвое выше соответствующих частот в хлорсиланах и близки к частотам атома хлора, связанного с серой. [4]
Характер гибридизации атомов цикла можно определить не только на основании КССВ 1ЭС - Н, как было показано выше, но и другими спектральными методами. [5]
 |
Схема ( / 3 -гибридиза-ции атома углерода.| Схема строения молекулы этилена С2Н4. [6] |
В этой форме гибридизации атома углерод образует свою вторую аллотропическую форму - графит. Кристаллическая решетка графита рассмотрена выше ( см. гл. Один атом углерода, обладая такой системой орбиталей, не может образовать устойчивую молекулу углеводорода, и поэтому два атома С соединяются между собой, замыкая а - и л-связь и заполняя остальные а-связи атомами водорода. Образуется мо: лекула этилена С2Н4 - простейшего непредельного водорода. [7]
В этой форме гибридизации атома углерод образует свою вторую аллотропическую форму - графит. Кристаллическая решетка графита рассмотрена выше ( см. гл. [8]
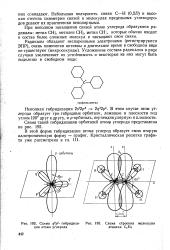 |
Схема ( рр1 - гибридиза - [ IMAGE ] Схема строения молекулы ции атома углерода этилена С2Н4. [9] |
В этой форме гибридизации атома углерод образует свою вторую аллотропическую форму - графит. Кристаллическая решетка графита уже рассмотрена в гл. [10]
С учетом состояния гибридизации атома кислорода в сульфо-ксидах и расстояния, на которое он удален от заместителей при атоме углерода в а-положении, вероятность появления в случае а-галогензамещенных соединений эффектов поля, аналогичных наблюдаемым у карбонильных соединений, чрезвычайно мала. [11]
Химический сдвиг углерода существенно зависит от гибридизации атома. Атомы углерода, участвующие в образовании тройной связи ( sp - гибридизация), обнаруживаются в промежуточной области. На рис. 2.1 представлены диапазоны химических сдвигов для некоторых классов соединений. [12]
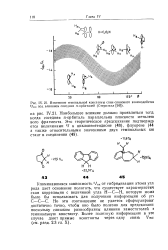 |
Изменение геминальной константы спин-спинового взаимодействя 2 / нн под влиянием соседних я-орбиталей ( Стернхелл. [13] |
Упоминавшаяся зависимость 2 / Нн от гибридизации атома рода дает основание полагать, что существует характеристич екая корреляция с величиной угла Н - С - Н, которую мож. Но это соотношение не удается сформулирова достаточно точно, чтобы оно было полезно для предсказани поскольку слишком разнообразны влияния заместителей f геминальную константу. Более полезную информацию в это случае дают прямые константы через одну связь ( см. разд. [14]
 |
Радиус эффективного действия молекулы хлора. [15] |
Страницы: 1 2 3 4 5