Гибридизация - атом
Cтраница 2
Ковалентные радиусы атомов являются функцией состояния гибридизации атома и типа орбитали. Обычно с усилением s - харак-тера гибридной орбитали ковалентный радиус уменьшается. [16]
Структура кова-лентных координационных кристаллов определяется характером гибридизации атомов ( стр. [18]
Однако для многих молекул однозначная интерпретация характера гибридизации атома фосфора представляется затруднительной. Так, в трехкоординационных соединениях фосфора с пирамидальной конфигурацией связей ( р3) валентные углы при атоме Р оказываются ближе к 100, нежели к идеальному значению 90, что может быть связано с определенным вкладом s - орбитали. Поэтому данные молекулы рассматривают также как тетраэдрические ( sp3) с неподеленной парой электронов, занимающей четвертую позицию. При этом, разумеется, нельзя исключить и влияние на величины валентных углов пространственных факторов. То же относится и к структурам с пятерной координацией атома Р, поскольку в ряде случаев искажения геометрии оказываются настолько велики, что координация лучше всего описывается как промежуточная между тригональ-но-бипирамидальной и тетрагонально-пирамидальной. [19]
Одновременно с делокализацией электронов происходит и изменение состояния гибридизации атома кислорода, который первоначально был связан с реакционным центром. [20]
Как мы видели ранее, орбитальная электроотрицательность зависит от гибридизации атома. Для уточнения представлений об орбитальной электроотрицательности, а также для описания связи между гибридизацией и электроотрицательностью было введено понятие регибридизации или нецелочисленной гибридизации. [21]
Как мы надели ранее, орбитальная эдектроогрнцагельность зависит от гибридизации атома. [22]
Наблюдаемый в ординарных связях парамагнетизм может также варьировать из-за различия в гибридизации атомов, образующих данную связь в зависимости от окружающих условий. По-видимому, следует ожидать, что более глубокое исследование этого весьма чувствительного парамагнетизма ординарных связей могло бы пролить свет на особенности гибридизации атомов в тех или иных случаях. [23]
 |
Параметры насыщенных трехчленных циклов 1 н их энергии напряжения. [24] |
Эффект напряжения валентных углов в этих соединениях сведен к минимуму изменением гибридизации атомов, составляющих кольцо. [25]
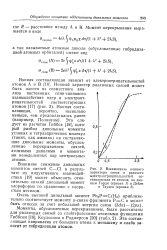 |
Взаимосвязь ионного. [26] |
Эта составляющая направлена от большего атома к меньшему и слабо зависит от гибридизации атомов. [27]
Очевидно, что и этот фактор сводится к двум уже рассмотренным - гибридизации атомов и делокализгции электронов, как его и трактовали Дьюар и другие авторы. [28]
 |
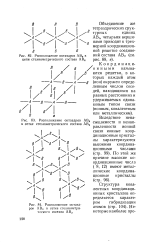
Каркас молекулы PF5 ( а и ее объемное изображение ( б. [29] |
Образующимся пяти связям Р - F в молекуле PF5 отвечает р3й - гибридизация атома фосфора, так как только путем передачи одного из электронов на Зс. Гибридизации spad отвечает геометрия тригональной бипирамиды ( рис. 11.27, а), которая задает валентные углы этой молекулы. [30]
Страницы: 1 2 3 4 5