Гибридизация - атом
Cтраница 4
Робинсон с соавторами [109] и Стевенс [ НО ] пытались объяснить природу возникновения координационных связей - гибридизацией атома иода. Вследствие вандерваальсовых сил между соседними атомами иода, возможно, происходит смешение spzdzz и р Д - орбиталей. Это смещает экстремальные направления электронной плотности ближе к направлениям связей. [46]
Как правило, гибридные орбита-ли данного атома в молекуле относятся к одному типу, к-рый называют типом гибридизации атома. [47]
Сравнение частот последних с частотами ЯКР 35С1 К К-дихлораминов жирного ряда [68] позволяет сделать вывод об изменении гибридизации атома asofa и его орбитальной заселенности. [48]
Автором были рассчитаны rs - и гр-радиусы s - и р-орбит для элементов первых четырех периодов, причем для определения гибридизации атомов использованы ядерные квадрупольные постоянные и известные с точностью 0 005 А и большей межатомные расстояния. [49]
Валентный угол С-О - С соответствует 112 для СНзОСНз, что близко к тетраэдрическому углу и указывает на лр3 - характер гибридизации атома кислорода. Простые эфиры относятся к числу малореакциоииоспособных веществ и стабильны по отношению ко многим реагентам ( металлоорганическим соединениям и др.), но они чувствительны по отношению к кислороду и легко образуют взрывчатые гидропероксиды, которые являются причиной взрыва при неосторожном обращении. [50]
В качестве примера, когда торсионные эффекты, по-видимому, играют главную роль, можно привести реакции, в которых происходит изменение гибридизации атомов в цикле. [51]
Уже в статье Коулсона [44] были сформулированы факторы, которые могут влиять на геометрические параметры молекул, наряду с порядками связей и гибридизацией атомов. [52]
При увеличении числа атомов фтора в фторхлорметанах Xo ( C) увеличивается, и для того чтобы выполнить условие согласования у, sp - гибридизация атома хлора должна увеличиваться. Одновременно увеличение Xc ( Q означает уплотнение ( уменьшение), орбитали углерода по величине, так что величина s, необходимая для максимального перекрытия, уменьшается. Таким образом, абсолютная величина sp - гибридизации увеличивается, но скорость увеличения убывает. [53]
Валентный угол С - О - С соответствует 1 12 для СН3ОСН3, что близко к тет-раэдрическому углу и указывает на sp - характер гибридизации атома кислорода. Простые эфиры относятся к числу малореак-ционноспособных веществ и стабильны по отношению ко многим реагентам ( металлоорганическим соединениям и др.), но они чувствительны по отношению к кислороду и легко образуют взрывчатые гидропероксиды, которые являются причиной взрыва при неосторожном обращении. [54]
Угол С - Sn-С 110 7 близок к тетраэдрическому, на основании чего и было предложено описывать [145] связи в комплексе, основываясь на зр3 - гибридизации атома олова и его трехцент-ровых связях с хелатными лигандами. Таким образом, описание строения даже этого комплекса на основе только s - и р-орбиталей атома олова не вполне удовлетворительно. В ряде же случаев, как показано выше, оно, по-видимому, вообще неприемлемо. [55]
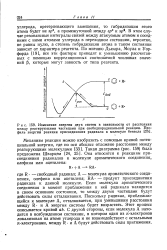 |
Изменение энергии двух систем в зависимости от расстояния между реагирующими частицами при свободнорадикальной реакции. Профиль энергии реакции присоединения радикала к молекуле бензола. [56] |
В этом случае резонансные интегралы связей между атакуемым атомом и соседними с ними атомами углерода в переходном состоянии, вероятно, не равны нулю, а степень гибридизации атома в таком состоянии зависит от характера реагента. По мнению Дьюара, Моула и Уор-форда [19], все эти факторы приводят к уменьшению рассчитанных с помощью корреляционных соотношений числовых значений Р, которые могут зависеть от типа реагента. [57]
В первом случае структура содержит плоские группировки [ ВОз ] с атомом бора в вр гибридном состоянии, во втором - тетраэдрические образования [ BOJ с - гибридизацией атома бора. [58]
В основе ее по-прежнему лежит уравнение (4.7), а также следующие два предположения: ( 1) длина связи и энтальпия связи X-Y определяются только сортами и гибридизацией атомов X и Y; ( 2) между энтальпией и длиной связей имеется взаимнооднозначное соответствие. [59]
В первом случае структура содержит плоские группировки [ ВО3 ] с атомом бора в р2 - гибридном состоянии, во втором - тетраэдрические образования [ ВО4 ] с - гибридизацией атома бора. [60]
Страницы: 1 2 3 4 5