Гибридизация - атом
Cтраница 3
В о-радикалах неспаренный электрон остается на а-орбитали, которая вследствие этого сохраняет гибридизацию атома, являющегося радикальным центром. [31]
Отклонение значений для связей и валентных углов от нормальных значений для соответствующих типов гибридизация атомов. [32]
 |
Строение тетрамерных фосфазенов. [33] |
Углы между связями отвечают sp2 - гибридизации орбиталей атомов азота и р3 - гибридизации атомов фосфора. Канонические формы составлены аналогично бензольному циклу, но в отличие от бензола л-связывание в фос-фазенах включает d - ря-взаимодействие. Это снижает устойчивость делокали-зованной молекулярной орбитали. [34]
Отклонение значений для связей и валентных углов от нормальных значений для соответствующих типов гибридизации атомов. [35]
Отклонение значений для связей к валентна углов от нормальных значений для соответствующих типов гибридизации атомов. [36]
Отклонение значений для связей и валентных углов от нормальных значений для соответствующих типов гибридизации атомов. [37]
Этот эффект должен проявляться лишь в тех случаях, когда реакция сопровождается изменением гибридизации атомов в основной цепи полимера, и, очевидно, не имеет места в реакциях, которые не связаны с изменением структуры полимерной цепи. [38]
Ван-дер-ваальсово взаимодействие ( отталкивание) между заместителем и син-аксиальными водородами уменьшается по мере изменения гибридизация атома С-2 от sps к рй. При пространственно более затрудненных алкильных группах энергия основного состояния повышается боль ше, чем энергия переходного состояния. [39]
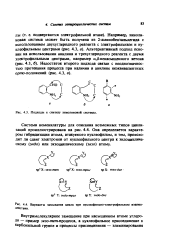 |
Подходы к синтезу хииолииовой системы.| Варианты замыкания цикла при иуклеофильио-электрофильиом взаимодействии. [40] |
Система номенклатуры для описания возможных типов циклизаций проиллюстрирована на рис. 4.4. Она определяется характером гибридизации атома, атакуемого нуклеофилом, и тем, происходит ли сдвиг электронов от нуклеофильного центра к эндоцикличе-скому ( эндо) или экзоциклическому ( экзо) атому. [41]
Вклад в энергию перестройки, обусловленный изменением энергии о-связи в связи М-X при изменении гибридизации атома бора или алюминия, в каждом случае сравнительно невелик и равен приблизительно 0 3 ккал / моль. Его можно грубо оценить, используя относительные величины о-перекры-вания в двух гибридных состояниях атома. [42]
Наоборот, Баки Хансен-Нигард [61] доказывают, что вариации в длинах связей обязаны совместному влиянию гибридизации атомов, делокализации электронов и еще некоторых факторов, природа которых пока не установлена. По мнению этих авторов, сбрасывать полностью со счетов фактор делокализации электронов ( как это делают Дьюар и Браун) нельзя, и они поставили целью исследовать, насколько длины связей зависят от влияния обоих этих факторов. [43]
Важным следствием из этого принципа является то, что энергии связи должны изменяться при изменении гибридизации АО участвующих атомов. Его 2s - AO по энергии находится гораздо ниже, чем 2р - АО. [44]
Рано или поздно вы встретитесь с такой практической задачей: как по структурной формуле определить состояние гибридизации атомов в молекуле данного соединения. [45]
Страницы: 1 2 3 4 5