Жидкий гидрат
Cтраница 2
Основной недостаток формулы ( 43) очевиден - жидкий гидрат принимается за вполне устойчивое соединение, не способное к диссоциации. В действительности жидкие гидраты ионов являются весьма непрочными, легко диссоциирующими комплексными соединениями. [16]
Рассмотрим случай раствора I-I электролита, катион которого образует жидкий гидрат, способный к диссоциации, характеризуемый целым гидратным числом п и константой нестойкости К. [17]
Для электролитов, один из ионов которых способен образовывать жидкие гидраты, величина ех доходит до 150е и выше. Следует отметить, что численное значение Е1 для этих электролитов существенно зависит от принятых нами представлений о гидратации ионов и характере диссоциации жидких гидрато ионов. Мы исходили [27] из координационного числа 4 и простейшего-представления о том, что жидкие гидраты диссоциируют не ступенчато, а от них отщепляются сразу все четыре молекулы воды. Если исходить из другого координационного числа или если учесть ступенчатый характер диссоциации, то численные значения констант а и 6 и величины кг существенно изменятся. [18]
Вторым приближением явилось [9, 17] более сложное предположение, что жидкие гидраты ионов I-I электролитов имеют одинаковое координационное число ( 4) и способны к диссоциации. [19]
Весьма вероятно, что в растворе сосуществуют одновременно несколько жидких гидратов одного и того же иона с различными гидрат-ными числами и что процесс диссоциации имеет ступенчатый характер, причем каждая ступень имеет свою константу нестойкости. Рассмотрим основные термодинамические соотношения для раствора, состоящего из свободных молекул воды, свободных ионов двух сортов и некоторого числа i различных жидких гидратов ионов. [20]
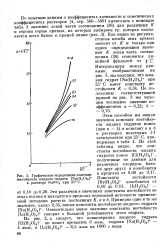 |
Графическое определение констант. [21] |
Из рис. 2, а следует, что концентрация жидкого гидрата [ С1 ( Н20) 4 ] - не может превысить 6 моль, гидрата [ Na ( H20) 4 ] - 4 моль, a [ Li ( H20) 4 ] - 8 5 моль на 1000 г воды. [22]
Как уже указывалось, предложенный нами метод определения констант нестойкости жидких гидратов ионов не претендует на большую точность, тем более что в основе его лежит условное предположение, что все гидраты имеют один и тот же состав с 4 молекулами воды. Поэтому необходимой предпосылкой дальнейшего развития гидратной теории растворов является разработка методики экспериментального определения концентрации свободной воды и жидких гидратов ионов. [23]
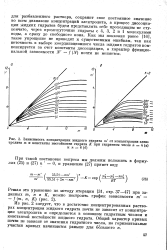 |
Зависимость концентрации жидкого гидрата т от концентрации электролита т и константы нестойкости гидрата К при гидратном числе п 4 ( а. [24] |
Из рис. 2 следует, что в достаточно концентрированных растворах концентрация жидкого гидрата почти не зависит от концентрации электролита и определяется в основном гидратным числом и константой нестойкости жидкого гидрата. [25]
Рассмотрим наиболее общий случай раствора электролита, когда оба его иона образуют жидкие гидраты состава [ A ( H2O) nJ и [ R ( H2O) na ] -, которые частично диссоциированы. [26]
Рассмотрим наиболее общий случай раствора электролита, когда оба его иона образуют жидкие гидраты состава [ А ( Н2О) Л1 ] и [ R ( H2O) n2 ] -, которые частично диссоциированы. [27]
Некоторая часть ионов А вступает в комплексное соединение с водой и образует жидкий гидрат A - nJi O, характеризуемый гидратным числом па и константой нестойкости Ка. [28]
В концентрированных растворах сильных электролитов термостатическими индивидумами могут быть свободные молекулы воды, жидкие гидраты ионов различного стехиометрического состава, негидратированные ( в смысле образования химических соединений с водой) ионы, недиссоциированные молекулы электролита и ионные ассоциаты стехиометрического состава. [29]
Было показано, что структуры этих веществ в целом аналогичны структуре газовых или жидких гидратов, но отличаются в деталях. Некоторые соединения фактически изострук-турны первой из описанных выше кубических структур газовых гидратов, но существуют и тетрагональные, орторомбические и моноклинные структуры. Катионы и части анионов ( например, часть С6Н5С бензоат-иона) заполняют полости редко и лишь случайно. [30]
Страницы: 1 2 3 4