Жидкий гидрат
Cтраница 4
Наиболее простой вид эта формула принимает в случае, когда мы имеем дело с раствором электролита, ионы которого не образуют жидких гидратов. [46]
Как мы показали ранее [16], такое упрощение не приводит к существенным ошибкам, так как неточность в выборе координационного числа жидких гидратов компенсируется за счет константы диссоциации, а характер функциональной зависимости N / ( N) почти не меняется. [47]
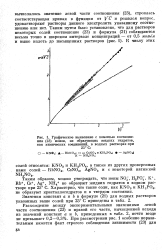 |
Графическое выявление с помощью соотношения ( 23 ионов, не образующих жидких гидратов, как химических соединений, в водных растворах при 25 С. [48] |
Таким образом, можно утверждать, что ионы N03, Н2РО, К, Rb, Cs, Ag, NH4 не образуют жидких гидратов в водном растворе при 25 С. Характерно, что такие соли, как RN03 и КН2Р04, не образуют кристаллогидратов и в твердом состоянии. [49]
Если учитывать все возможные гидратные формы, то построение количественной теории растворов электролитов становится практически невозможным из-за громоздкости формул и неопределенности значений констант нестойкости жидких гидратов. Поэтому в гидрат-ной теории растворов, развиваемой Г. И. Микулиным [3], принято для упрощения, что координационное число не изменяется во всем диапазоне концентраций, сохраняя свое значение, характерное для разбавленного раствора, процесс диссоциации жидких гидратов проходит не ступенчато, а сразу до свободного иона. Это допущение оправдывается тем, что неточность в выборе координационного числа компенсируется за счет константы нестойкости, а характер зависимости количества жидких гидратов от концентрации электролита почти не меняется. [50]
Логарифмический член формулы ( 5) исчезнет при дифференцировании и в том случае [17], когда в растворе присутствуют не два, а любое число жидких гидратов ионов, каждый из которых характеризуется целым гидратным числом и константой нестойкости, причем, последняя зависит от температуры и давления. Не следует, однако, думать, что при этом исчезнет всякое влияние химической гидратации на объемные и тепловые свойства раствора. [51]
Подставляя их в формулу ( 15), найдем значение свободной энтальпии раствора в зависимости от концентрации электролита, гидратных чисел п ( и констант нестойкости Kt жидких гидратов ионов. К сожалению, это неосуществимо из-за недостатка экспериментальных данных, так как все обычные методы, которыми пользуются для определения составов комплексов и констант нестойкости, неприменимы к жидким гидратам ионов. [52]
Как показали наши расчеты, форма кривых NT f ( N) мало зависит от гидратного числа и не меняется существенно даже в том случае, если диссоциация жидких гидратов происходит ступенчато - через промежуточные гидраты. [53]
Страницы: 1 2 3 4