Жидкий гидрат
Cтраница 3
Рассмотрим три ( постепенно усложняющихся) варианта такой теории: ионы не образуют жидких гидратов определенного стехио-метрического состава; такой гидрат образует один из ионов; оба иона образуют жидкие гидраты. [31]
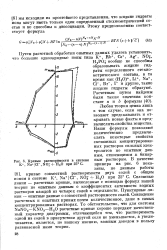 |
Кривые растворимости в системе К, Na Cl-NOj H20 при 25 С. [32] |
Li, Na, СГ, Вг -, I и другие, такие жидкие гидраты образуют. Любая теория ценна лишь в том случае, если она позволяет предсказывать и открывать новые факты и пред-вычислять свойства вещества. [33]
Перейдем к рассмотрению наиболее общего случая раствора I-I электролита, оба иона которого образуют жидкие гидраты [ A ( H20) BJ и [ ЩН20) И2 ] -, частично диссоциирующие с образованием свободных ионов А и R - и свободных молекул воды. [34]
Это объясняется, по нашему мнению, тем, что ионы С1 - зуют жидкие гидраты ионов типа [ С1 ( Н20) 4 ] -, а ионы N03 гидратов не образуют. [35]
Как показано в работе [47 ], описанное выше второе приближение теории, учитывающее диссоциацию жидких гидратов ионов, не дает особого улучшения по сравнению с первым приближением, применительно к расчету кривых растворимости в системе К, 1Ча С1 -, NOj H20 при 25 С. [36]
R образует жидкий гидрат R ( H2O) B, частично диссоциирующий с образованием другого жидкого гидрата R ( H20) / с меньшим гидратным числом. [37]
Степень гидратации ионов в растворах, таким образом, не постоянна, определяется константами нестойкости жидких гидратов и зависит от концентрации электролита в растворе. Как полагает автор [27], ионы К, Rb, Cs, NH NO -, Н2РО - не образуют жидких гидратов определенного стехиометричес-кого состава. Константы нестойкости жидких гидратов анионов мало зависят от природы присутствующего в растворе катиона. Это же справедливо и в случае катионов. [38]
Выше мы подробно разобрали различные формулы для свободной энтальпии раствора, учитывающие существование и диссоциацию жидких гидратов ионов. [39]
В работе [7] было использовано простейшее представление о том, что все иены каждого вида образуют жидкие гидраты лишь одного определенного состава, не зависящего от концентрации раствора, : не способные к диссоциации. [40]
С помощью уравнения ( 19) легко построить диаграмму зависимости NT f ( N) концентрации жидкого гидрата от концентрации электролита в растворе. Такая диаграмма для п 4 изображена на рис. 1 в виде серии изолиний, каждая из которых отвечает определенному значению константы нестойкости К. Из этой диаграммы наглядно видно, что с ростом концентрации раствора концентрация жидкого гидрата сначала пропорционально увеличивается, потом рост ее замедляется, и в крепких растворах концентрация жидкого гидрата остается практически постоянной, не зависящей от моляль-ности раствора. [41]
Таким образом, условие ( 43) соответствует предположению, что раствор электролита - это идеальный раствор жидких гидратов ионов и свободных молекул воды. [42]
В табл. 2 приведены вычисленные указанным выше путем ( по данным табл. 1) значения концентрации солей и жидких гидратов ионов и свойства растворов, насыщенных двумя солями. [43]
Вопрос о влиянии образования жидких гидратов на термодинамические свойства раствора разбирался Ван-Лааром [16], ошибочно утверждавшим, что степени диссоциации жидких гидратов носят фиктивный характер и могут быть взяты совершенно произвольно. В действительности константы диссоциации жидких гидратов являются объективно существующими величинами, которые, как мы сейчас увидим, входят в формулы для термодинамических свойств раствора. [44]
Предположение, что гидратное число п не зависит от концентрации раствора, не соответствует имеющимся данным и противоречит представлению о жидких гидратах как нестойких, диссоциирующих соединениях. [45]
Страницы: 1 2 3 4