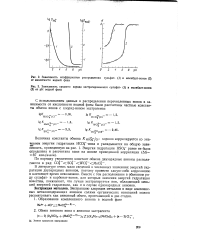
Гидратация - анион
Cтраница 2
Последовательность соответствует порядку возрастания энергии гидратации анионов. Это означает, что энергия сольватации имеет определяющее значение в электродной селективности этих систем. Корреляция потенциометрической ( электродной) и экстракционной ( сольватационной) селективности была проверена многими исследователями. [16]
Какой тип химической связи возникает при гидратации анионов и при каких условиях это приводит к их гидролизу. [17]
 |
Зависимость адсорбции ( / и адсорбционного скачка потенциала ( 2 на границе раствор - воздух от концентрации w - валериановой кислоты ( а и зависимость. [18] |
Данный ряд соответствует увеличению химической энергии гидратации анионов. [19]
В строке 9 приведены значения энтальпии гидратации анионов. [20]
 |
Зависимость адсорбции ( / и адсорбционного скачка потенциала ( 2 на границе раствор - воздух от концентрации w - валериановой кислоты ( а и зависимость. [21] |
Данный ряд соответствует увеличению химической энергии гидратации анионов. [22]
В большинстве исследованных систем различия между энергиями гидратации анионов оказывают определяющее влияние на относительную способность различных кислот экстрагироваться аминами. [23]
Отсутствие заметного дипольного момента обусловливает и отсутствие заметной гидратации аниона. Поэтому гидролизованные комплексные ионы Sb ( V) хорошо экстрагируются даже простыми эфирами. [24]
В отличие от катионов вопрос интерпретации изотоцных эффектов гидратации анионов представляется более сложным. Эти качественные изменения состава гидратной оболочки анионов приводят к количественному отличию их изотопных эффектов гидратации. Перенос галогенид-ионов в тяжелую воду сопровождается только положительными при 298 15 К значениями AHj н - d которые, как уже отмечалось, находятся в сильной зависимости от радиуса аниона и заметно преобладают по абсолютной величине над A - h - d катионов. Вероятно, здесь большую роль играет специфичность гидратации анионов, выражающаяся в их способности образовывать с молекулами воды связи типа водородных, которые конкурируют по силе с водородными связями между молекулами воды. Это может служить одной из причин большего разрушающего действия анионов по сравнению с катионами. Таким образом, положительный знак Д / / н D анионов имеет двоякое происхождение из-за усиления разупорядочивающего действия анионов на структуру тяжелой воды и большей прочности дей-териевой связи, разрушение которой связано с более значительными энергетическими затратами. Эти вклады частично компенсируются отрицательным вкладом образования более прочной, чем в обычной воде, связи X... [25]
Если энтальпия гидратации катиона резко отличается от энтальпии гидратации аниона, то значения ДЯ С 0 и соответствующие соли будут хорошо растворимы в воде. [26]
По-видимому, такая зависимость экстракции кислот связана с гидратацией анионов и иона водорода в водных растворах этих кислот. [27]
Предполагают, что причиной понижения ККМ является увеличение степени гидратации аниона в данном ряду, приводящее к уменьшению концентрации противоионов в слое Штерна. [28]
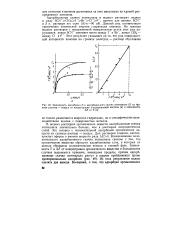
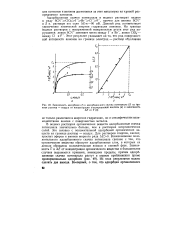
Учитывая сказанное, следует ожидать корреляции между значениями энергий гидратации аниона и константой экстракционного обмена: чем больше энергия гидратации, тем более энергетически затруднен переход аниона в органическую фазу. На рис. 1 представлена зависимость констант обмена исследованных анионов от разности энергий гидратации этих ионов. Значения энергий гидратации взяты из монографии Измайлова. Как видно, наблюдается удовлетворительная линейная корреляция, включающая данные по обмену девяти анионов. Установленная корреляция позволяет определять энергии гидратации и для других однозарядных анионов. [29]
Страницы: 1 2 3 4