Гидратация - анион
Cтраница 3
В литературе очень мало сведений о численных значениях энергий гидратации двузарядных анионов, поэтому провести какую-либо корреляцию в настоящее время невозможно. Вместе с тем расположение в обменном ряду сульфат - и карбонат-ионов, для которых значения энергий гидратации известны, показывает, что лучше экстрагируется ион, обладающий меньшей энергией гидратации, как и в случае однозарядных анионов. [31]
 |
Энтропия молекул воды в ближайшем окружении ионов ( а и коэффициент вязкости В в уравнении Джонсона-Дола ( б. [32] |
Отмеченное ион-дипольное взаимодействие наиболее характерно для гидратации катионов, при гидратации анионов со значительным зарядом или малым радиусом более типично присоединение молекул воды за счет водородных связей. [33]
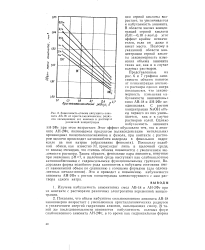 |
Зависимость объема набухшего анионита АВ-18 от кристаллохимических радиусов насыщающих его анионов в растворах различной концентрации. [34] |
АВ-18 закономерно возрастает с уменьшением кристаллохимических радиусов и увеличением энергий гидратации анионов, насыщающих смолу. [35]
Второй путь экстракционной очистки солей щелочных металлов может быть основан на уменьшении энергии гидратации анионов путем введении в последние различных гидрофобных групп. [36]
Гсоли должно обусловливаться не только изменением степени гидратации катиона, но и степени гидратации аниона. [37]
Второй способ экстракционной очистки солей щелочных металлов может быть основан на уменьшении теплоты гидратации анионов путем введения в последние различных гидрофобных групп при сохранении величины U постоянной. К сожалению, число исследований, посвященных изучению этого вида экстракционного разделения щелочных металлов, крайне ограничено. [38]
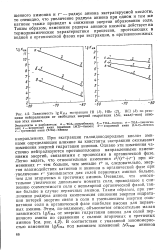 |
Зависимость IgKnA экстракции HI ( 1, НВг ( 2, НС1 ( 3 по реакциям нейтрализации от свободных энергий гидратации ( ДО, ккал / г-ион анионов этих кислот. [39] |
При экстракции галоидоводородных кислот аминами определяющее влияние на константы экстракции оказывают изменения энергий гидратации анионов. Однако эти изменения частично нейтрализуются противоположно направленными изменениями энергий, связанными с процессами в органической фазе. Легко видеть, что относительные изменения е2 / ( г - - г -) при изменениях г - тем больше, чем меньше г и, следовательно, энергия взаимодействия катионов и анионов в органической фазе при увеличении г - уменьшается для солей первичных аминов больше, чем для вторичных и третичных аминов. Очевидно, что относительное увеличение дипольного момента соли, приводящее к снижению совместимости соли с неполярной органической фазой также больше в случае первичных аминов. Таким образом, при увеличении радиуса аниона компенсация снижения энергии гидратации потерей энергии связи в соли и уменьшением энергии сольватации соли в органической фазе наиболее высока для первичных аминов. [40]
Как видно из рис. 3 - 6, наблюдается также зависимость коэффициента распределения от параметров, характеризующих гидратацию анионов и влияние их на структуру водных растворов. [41]
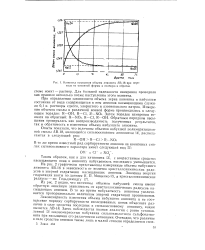 |
Кинетика изменения объема анионита АВ-18 при переходе из основной формы в солевую и обратно. [42] |
На рис. 2 графически представлены измеренные объемы набухшего анионита АВ-18 в зависимости от величин кристаллохимических радиусов и энергий гидратации насыщающих анионов. [43]
 |
Экстракция технеция полярными растворителями. [44] |
Извлечение ионных ассоциатов Тс ( VII) зависит от природы высаливающих кислот и солей, их концентрации и характера гидратации аниона. [45]
Страницы: 1 2 3 4