Гидратация - соль
Cтраница 2
Имеется множество экспериментальных данных о тепло-тах гидратации солей, которые совпадают между собой в пределах десятых долей процента. В то же время имеющиеся данные для отдельных ионов сильно отличаются между собой. Это различие не является результатом экспериментальных ошибок, а следствием различных методов стандартизации. Вероятно, наиболее надежными являются данные о теплотах, эктропиях и энергиях сольватации, полученные в результате совместного рассмотрения этого вопроса школой Мищенко, школой Капустинского и школой Яцимирского. [16]
Имеется множество экспериментальных данных о теплотах гидратации солей, которые совпадают между собой в пределах десятых долей процента. В то же время имеющиеся данные для отдельных ионов сильно различаются между собой, что не является результатом экспериментальных ошибок, а следствием разных методов стандартизации. [17]
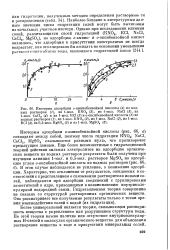
На рис. 2 показана зависимость теплоты гидратации солей от аниона галогена и от катиона щелочного металла. [18]
Достигаемое при повышении температуры ускорение процесса гидратации соли чаще всего компенсируется уменьшением степени гидратации за счет повышения давления паров воды над солью. [19]
Имеется множество экспериментальных данных о теплотах гидратации солей, которые совпадают между собой в пределах десятых долей процента. В то же время имеющиеся данные для отдельных ионов сильно различаются между собой, что не является результатом экспериментальных ошибок, а следствием разных методов стандартизации. Вероятно, наиболее надежными являются данные о теплотах, энтропиях и энергиях сольватации, полученные в результате совместного использования школы Мищенко, школы Капустин-ского и школы Яцимирского. [20]
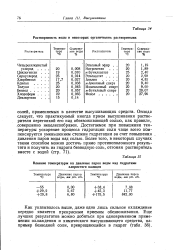 |
Растворимость воды в некоторых органических растворителях. [21] |
Достигаемое при повышении температуры ускорение процесса гидратации соли чаще всего компенсируется уменьшением степени гидратации за счет повышения давления паров воды над солью. [22]
Отсюда совершенно ясно, что теплота гидратации хлорной соли больше, чем бромной. [23]
Наиболее близкие к литературным данным значения чисел гидратации солей могут быть вычислены из начальных участков изотерм. [25]
Нередко проявляется подобное же влияние воды на соль: гидратация соли сопровождается усилением полярности связи в ней. Так, безводный А1С13 не содержит ионов А13, так как отделение трех электронов от атома требует затраты слишком большой) количества энергии. [26]
Эйкен [135] на основе анализа опытных данных по теплотам гидратации солей показал, что закон постоянных разностей справедлив и для теплот гидратации соли. [27]
 |
Относительное расположение ионов металла и молекул воды в гидратах катионов ( а Li - 4H2O и ( б Mg2 - 6H2O - no Берналу. [28] |
Нередко проявляется и подобное же влияние воды на соль: гидратация соли - сопровождается усилением полярности связи в ней. Так, безводный А1С13 не содержит ионов А13, так как отделение трех электронов от атома требует затраты слишком большого количества энергии. В безводном А1СЦ связи ковалентные полярные, но при гидратации его степень ионности связей сильно возрастает за счет энергии процесса гидратации. [29]
 |
Относительное расположение ионов металла и молекул воды в гидратах катионов ( a Li 4Н2О и ( б Mg2 GHjO - по Берналу. [30] |
Страницы: 1 2 3 4