Гидратация - соль
Cтраница 3
Нередко проявляется и подобное же влияние воды на соль: гидратация соли сопровождается усилением полярности связи в ней. Так, безводный А1С13 не содержит ионов А13, так как отделение трех электронов от атома требует затраты слишком большого количества энергии. [31]
 |
Относительное расположение ионов металла и молекул воды в гидратах катионов ( а Li - 4H2O и ( б Mg2 - 6H2O - no Берналу. [32] |
Нередко проявляется и подобное же влияние воды на соль: гидратация соли сопровождается усилением полярности связи в ней. Так, безводный Aids не содержит ионов А13, так как отделение трех электронов от атома требует затраты слишком большого количества энергии. В безводном А1С13 связи ковалентные полярные, но при гидратации его степень ионности связей сильно возрастает за счет энергии процесса гидратации. [33]
По нашему мнению, эти данные не дают возможности судить о гидратации солей в органической фазе. [34]
При расчете теплот гидратации широко пользуются правилом, согласно которому разность теплот гидратации солей, содержащих какие-либо два иона, будет одной и той же независимо от того, с какими ионами противоположного знака они связаны. Это правило является следствием того, что теплота гидратации при бесконечном разведении представляет собой сумму теплот гидратации отдельных ионов. [35]
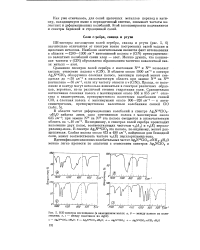 |
ИК-спектры поглощения ( в вазелиновом масле. а, б - между пленок из полиэтилена. в, г - между пластинок из AgCl о - Ag2N C10 - KH0. б - Ag N C10. a. H0. в - Ag N C10. г - Agj. [36] |
Правда, ее положение и контур могут несколько изменяться в спектрах различных образцов, вероятно, из-за различной степени гидратации соли. [37]
Эйкен [135] на основе анализа опытных данных по теплотам гидратации солей показал, что закон постоянных разностей справедлив и для теплот гидратации соли. [38]
Характерной особенностью экстракционных систем с органическими основаниями являются значительные положительные отклонения от идеальности в органической фазе, что объясняется ассоциацией и гидратацией солей. Вследствие этого термодинамическое описание таких систем затруднено, и многие наблюдаемые явления до последнего времени не находили правильного объяснения. [39]
Этим обстоятельством объясняется и упоминавшееся выше явление обращения рядов устойчивости аммиакатов у элементов с высокими значениями потенциалов ионизации и то, что теплота гидратации солей элементов побочных групп всегда ниже, чем солей главных групп, и, наконец, то, что теплота образования аммиакатов иодидов элементов главных групп периодической системы всегда больше, чем у иодидов элементов побочных групп. [40]
Несмотря на указанные недостатки выражения ( I, 22), нужно признать, что радиус иона безусловно представляет такую характеристику его, которая в значительной степени определяет величину с / г. Кривые рис. 2 показывают влияние радиуса ионов на теплоту гидратации солей. Радиус иона входит в уравнение ( I, 20), а в выражение для DQ входит расстояние между ионами, равное сумме радиусов их. Если допустить, что сольватация в основном связана с ориентацией диполей молекул растворителя вокруг иона, то естественно, что эта ориентация и энергия связи молекул растворителя с ионом должны определяться напряженностью поля вокруг иона. Последняя же зависит от заряда и радиуса его. [41]
 |
Интегральные теплоты растворения в воде при 20.| Схема к выводу тем - двумя путями. ACD и ABD. По пути ABD пературнои зависимости ОН. вначаде проводится реакция при температу. [42] |
Первая из них, как известно, равна 1440 калориям на 1 моль воды. Теплота гидратации солей зависит от количества присоединяемой воды и от природы соли. [43]
Определение теплоты гидратации соли сводится к определению теплот растворения безводной соли и ее кристаллогидрата. [44]
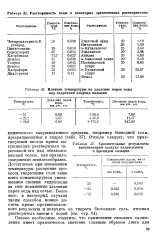 |
Растворимость воды в некоторых органических растворителях.| Влияние температуры на давление паров воды над гидратами хлорида кальция.| Сравнительные результаты. [45] |
Страницы: 1 2 3 4