Отрицательная гидратация
Cтраница 2
Если соль с повышением температуры переходит из области отрицательной гидратации в область положительной гидратации, то происходит также инверсия температурного хода активности воды. [16]
Первый эффект был назван деструктурирова-нием, а второй - отрицательной гидратацией. Если продолжать увеличивать заряд молекулы, то при достаточно высоком отношении между зарядом и радиусом частицы соседние молекулы растворителя оказываются жестко ориентированными в поле иона и образуют сольва-тационную оболочку, где атомы кислорода обращены к катиону, а атомы водорода - к аниону. [17]
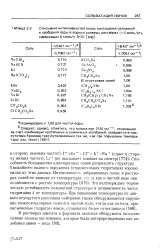 |
Отношения интенсивностей полос поглощения связанной. [18] |
Способность большинства однозарядных ионов разрыхлять структуру ближайшего водного окружения ( отрицательная гидратация) хорошо видна из этих данных. Это подтверждает термическую устойчивость сольватной структуры и независимость чисел гидратации h от температуры. [19]
С ионы 1Л гидратирова-лы положительно, тогда как для ионов К характерна отрицательная гидратация. Отрицательная гидратация ионов Na, наблюдаемая при низкой температуре, становится положительной при 26 5 С. В общем повышение температуры облегчает положительную гидратацию. Гидратация иона К при температуре примерно 80 - 100 С из отрицательной становится положительной, тогда как положительная гидратация иона Li при понижении температуры от - 10 до - 15 С изменяется на отрицательную. [20]
Таким образом, при одноименном катионе способность соли к ассоциации возрастает с увеличением отрицательной гидратации аниона. Интересно отметить, что согласно появившимся в самое последнее время данным [211], в водных растворах NaCl, KC1 и Csl ассоциированы. Полученные двумя различными методами значения К. [21]
Обычно р аниона pl Рно1 т - е - ани - оны преимущественно обладают отрицательной гидратацией. [22]
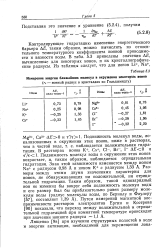 |
Измерение энергии ближайших молекул в окружении некоторых ионов. [23] |
Подвижность молекул воды в окружении этих ионов возрастает, и, таким образом, наблюдается отрицательная гидратация. Знак этой зависимости изменяется между ионом Na с радиусом 0 98 А и ионом К с радиусом 1 33 А. Размеры между этими двумя значениями характерны для ионов, не обнаруживающих ни положительной, ни отрицательной гидратации. Путем измерений магнитной восприимчивости растворов электролитов Ергин и Кострова [96] показали, что переход между положительной и отрицательной гидратацией три комнатной температуре происходит при значении ионного радиуса - 1 1 А. [24]
В соответствии с представлениями Самойлова обмен молекул воды в первичной гидратной оболочке, включая и отрицательную гидратацию, не противоречит тому факту, что гидратация представляет собой сильно экзотермический лроцесс. Согласно этой теории, главная часть энергетического эффекта обусловлена вторичной гидратацией, связанной с более далекими молекулами воды. [25]
Коэффициент самодиффузии воды в растворах КС1 и KJ ( электролиты, составленные из ионов только с отрицательной гидратацией) оказался больше, чем в чистой воде. [26]
В настоящее время приведенные результаты ( высокие значения частот обмена ближайших к ионам молекул воды раствора, существование отрицательной гидратации, указанная граница между положительной и отрицательной гидратацией) довольно широко подтверждены экспериментально рядом методов и прежде всего методом ядерного магнитного резонанса, методом инфракрасной спектроскопии, а также энтропийными и теплоемкостными характеристиками ионов в бесконечно разбавленных водных растворах. [27]
В свете представлений о той, что натрий и калий является ионами, лежащими по обе стороны границы положительной я отрицательной гидратации, можно считать, что в количественном отношении энергии связи этих катионов с молекулами воды мало отличаются от энергии водородной связи в чистой воде. Поэтому энтальпия конденсации таких гаэогидратов может быть близка к энтальпии конденсации шести молекул воды. [28]
Я - Самойлов в книге Структура водных растворов электролитов и гидратация ионов сформулировал кинетическую теорию гидратации ионов и ввел понятие об отрицательной гидратации. [29]
В общем можно показать, что в разбавленных водных растворах число молекул воды с подвижностью, измененной под влиянием положительной или отрицательной гидратации катионов, приблизительно не зависит от природы анионов. [30]
Страницы: 1 2 3 4