Отрицательная гидратация
Cтраница 3
Химические добавки, такие, как КС1, NH4C1, KNO3, NH4NO3 и KJ, в которых содержатся ионы с отрицательной гидратацией, снижают вязкость воды. В результате экранирования сил притяжения и отталкивания и снижения вязкости воды на поверхности цементных частиц образуются тонкие сольватные оболочки ( практически адсорбционный слой) со значительно меньшей плотностью воды, чем при обычной гидратации твердой фазы. Вместе с этим облегчается сближение частиц под влиянием нормального давления, сопутствующего уплотнению цементного геля. Такие явления придают твердой фазе свойства гидрофобных коллоидов, снижают ее адсорбционную способность и резко повышают растворяющую функцию воды, ускоряющую диссоциацию минералов цемента на ионы. [31]
 |
Концентрационная зависимость рефракций электролитов. [32] |
Ионы Li, Na, Ca2 и Sr2 обладают положительной гидратацией, ионы К, Rb, Ch, В г - и I - - отрицательной гидратацией. Сумма энергий ближней гидратации различных комбинаций ионов может быть как положительной, так и отрицательной и в результате растворение тех или иных солей может как укреплять, так и ослаблять водородные связи в воде. Конкретно соли калия, наиболее часто рассматриваемые в данной книге соединения, дают суммарный отрицательныii эффект, поэтому их растворение в воде должно сопровождаться ломкой водородных связей и, следовательно, понижением рефракции. Аналогично, хотя и в меньшей степени, должны понижать рефракцию при растворении в воде соли натрия. [33]
Ионы Li, Na, Ca2 и Sr2 обладают положительной гидратацией, ионы К, Rb, C1 -, В г - и I - - отрицательной гидратацией. Сумма энергий ближней гидратации различных комбинаций ионов может быть как положительной, так и отрицательной и в результате растворение тех или иных солей может как укреплять, так и ослаблять водородные связи в воде. Конкретно соли калия, наиболее часто рассматриваемые в данной книге соединения, дают суммарный отрицательный эффект, поэтому их растворение в воде должно сопровождаться ломкой водородных связей и, следовательно, понижением рефракции. [34]
Рассмотренные представления о структуре воды и водных растворов электролитов, а также новый подход к изучению гидратации ионов в водных растворах ( и, в частности, представление 66 отрицательной гидратации) безусловно должны быть использованы при выяснении сущности таких физико-химических процессов, Как процессы выщелачивания и растворения горных пород Подземными водами. [35]
Следует отметить, что отрицательные дифференциальные теплоты сорбции калиевой, цезиевой и таллиевой форм ионита наблюдаются только после сорбции первых четырех молей воды, именно тогда, когда создаются предпосылки для проявления эффекта отрицательной гидратации. Последняя может осуществляться лишь под влиянием сформировавшегося порядка дальней гидратации, как следует из современной теории гидратации. [36]
Калий я цезий имеют одинаковую энергию диссоциации хлоридов, а в случае цезиевой формы теплота сорбции первых молей воды меньше, чем для калия, что согласуется с наличием большего ионного радиуса и соответственно большей отрицательной гидратации иона цезия. [37]
Влияние структурного состояния воды на гидратацию ионов ярко отражается в таких явлениях, как изменение гидратации ионов с температурой [77, 78], давлением [74] и под влиянием добавок неэлектролитов, солевые эффекты растворимости неполярных газов, наличие у ряда ионов отрицательной гидратации и зависимость границы между положительной и отрицательной гидратацией от температуры [75], давления, концентрации [76], добавок неэлектролита и изотопного состава воды. [38]
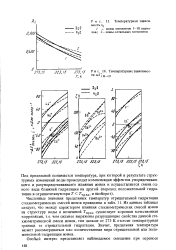 |
Температурные зависимос. [39] |
Из данных таблицы следует, что между характером влияния стехиометрических смесей ионов на структуру воды и величиной Тпреа существует хорошая качественная корреляция, т.е. чем сильнее выражены разрушающие свойства данной сте-хиометрической смеси ионов, тем дальше от 273 К отстоит температурная граница ее отрицательной гидратации. Значит, предельная температура может рассматриваться как количественная мера отрицательной или положительной гидратации ионов. [40]
С ионы 1Л гидратирова-лы положительно, тогда как для ионов К характерна отрицательная гидратация. Отрицательная гидратация ионов Na, наблюдаемая при низкой температуре, становится положительной при 26 5 С. В общем повышение температуры облегчает положительную гидратацию. Гидратация иона К при температуре примерно 80 - 100 С из отрицательной становится положительной, тогда как положительная гидратация иона Li при понижении температуры от - 10 до - 15 С изменяется на отрицательную. [41]
В первом случае ослабляется трансляционное движение молекул воды вблизи иона, они становятся менее подвижными, чем в чистой воде. При отрицательной гидратации, наоборот, возрастает подвижность молекул воды вблизи иона. [42]
Из сказанного следует, что при Т Гпред предельный радиус равен радиусу того иона, для которого определена предельная температура. Граница перехода отрицательной гидратации в положительную смещается с ростом температуры в сторону больших радиусов за счет уменьшения взаимной связанности молекул воды и усиления взаимодействия их с ионами при увеличении температуры. При переходе от Н2 О к D2 О зависимость г пред от температуры в общем сохраняется в прежнем виде, но изменения становятся более резкими, и в случае анионов граница пред смещается в сторону меньших радиусов. [43]
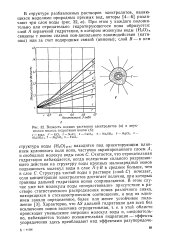 |
Вязкость водных растворов электролитов ( а и двух-зонная модель гидратации ионов ( б. [44] |
Считается, что отрицательная гидратация наблюдается, когда вследствие сильного разрушающего действия на структуру воды крупных малозарядных ионов подвижность молекул воды в слое А - - В в среднем больше, чем в слое С. Структура чистой воды в растворе ( слой С) исчезает, если концентрация электролитов достигает величин, при которых границы дальней гидратации ионов соприкасаются. [45]
Страницы: 1 2 3 4