Ближняя гидратация
Cтраница 2
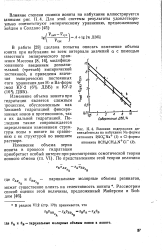 |
Влияние содержания ди-винилбензола на набухание Na-формы катионита RSO - Na ( 1 и Cl-формы. [16] |
Изменение объема ионита при гидратации является сложным нроцессом, обусловленным как ближней гидратацией фиксированных ионов и противоионов, так и их дальней гидратацией. [17]
Рассмотренные два вида взаимодействий не являются взаимоисключающими, они, описывая единый сложный процесс ближней гидратации ионов, дополняют друг друга. Так, Крестов [3], рассчитывая суммарное изменение энтропии воды ( А5ц) в растворах электролитов, подтвердил правомочность гипотезы об отрицательной ( энтропия системы возрастает и ASn0) и положительной ( энтропия системы уменьшается Д5ц0) гидратации ионов. В первом случае преобладает эффект разупорядо-чения структуры воды, во втором - эффект упорядочения. Из ионов, присутствующих в природных водах, ионы К, имеющие большой радиус и малый заряд, оказывают разупорядыва-ющее действие, а многозарядные катионы Са2, Mg2 и многоатомные анионы НСО3 - и SO42 - - упорядочивают структуру воды. [18]
 |
Гидратация ионов в растворе ( а, энтропия молекул воды в ближайшем окружении ионов ( б и коэффициент вязкости в уравнении Джонсона-Дола ( в. [19] |
Рассмотренные два вида взаимодействия не являются взаимоисключающими, они, описывая единый сложный процесс ближней гидратации ионов, дополняют друг друга. Так, Крестов, рассчитывая суммарное изменение энтропии воды ASn в растворах электролитов, подтвердил правомочность гипотезы об отрицательной ( энтропия системы возрастает и Д5И 0) и положительной ( энтропия системы уменьшается и ASIt 0) гидратации ионов. В первом случае преобладает эффект разупорядочения структуры воды, во втором - эффект упорядочения. Из ионов, присутствующих в природных водах, ионы К, имеющие большой радиус и малый заряд, оказывают разупорядочивающее действие, а многозарядные катионы Са2, Mg2 и многоатомные анионы НСО, SO - упорядочивают структуру воды. [20]
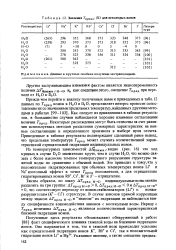 |
Значения Гпред ( К для некоторых ионов. [21] |
Полученные здесь результаты обосновывают обнаруженный в работе [88] факт специфического влияния тяжелой воды на ближнюю гидратацию ионов. [22]
В заключение необходимо указать на следующее: еще з 1967 году Борона и Самойлов [279] нашли, что данные по плотности водных растворов электролитов могут быть с успехом использованы для количественной характеристики ближней гидратации ионов в растворах. Изложенные здесь результаты полностью подтверждают их выводы. [23]
В работах О. Я. Самойлова показано, что гидратацию ионов следует в общем случае рассматривать не как связывание того или иного числа молекул воды, а как действие ионов на трансляционное движение прежде всего ближайших к ним молекул воды раствора. Ближняя гидратация ионов ( их взаимодействие с ближайшими молекулами воды раствора) может быть охарактеризована величинами А. [24]
Влияние ионов на структуру воды связано с их гидратацией. Различают ближнюю гидратацию ( взаимодействие иона с ближайшими к нему молекулами воды) и дальнюю гидратацию - поляризацию более отдаленных молекул воды. Характеристикой ближней гидратации является отношение времени пребывания молекулы воды в ближайшем окружении иона ко времени нахождения ее в положении равновесия с другими молекулами в невозмущенной структуре воды. На основании данных о растворимости солей и теплотах гидратации ионов установлено, что на связь одной молекулы с катионом в зависимости от его заряда ( 1, 2 или 3) приходится соответственно 42, 126 или 420 кДж / моль. В последнем случае гидратиро-ванный катион похож на химическое соединение. [25]
Влияние ионов на структуру воды связано с их гидратацией. Различают ближнюю гидратацию ( взаимодействие иона с ближайшими к нему молекулами воды) и дальнюю гидратацию - поляризацию более отдаленных молекул воды. Характеристикой ближней гидратации является отношение времени пребывания молекулы воды в ближайшем окружении иона ко времени нахождения ее в положении равновесия с другими молекулами в невозмущенной структуре воды. В последнем случае гидратированный катион похож на химическое соединение. [26]
Теория высаливания из водных растворов, сформулированная О. Я. Самойловым [168, 169], обобщает изложенный материал. Рассматривая изменение ближней гидратации высаливаемого катиона в растворе под влиянием высаливателя, О. Я. Самойлов нашел, что основное значение имеет ориентация молекул воды вблизи высаливаемого иона и изменение ее под действием ионов высаливателя. Катионы высаливателя уменьшают, анионы увеличивают ближнюю гидратацию высаливаемого катиона. [27]
Ионы Li, Na, Ca2 и Sr2 обладают положительной гидратацией, ионы К, Rb, C1 -, В г - и I - - отрицательной гидратацией. Сумма энергий ближней гидратации различных комбинаций ионов может быть как положительной, так и отрицательной и в результате растворение тех или иных солей может как укреплять, так и ослаблять водородные связи в воде. Конкретно соли калия, наиболее часто рассматриваемые в данной книге соединения, дают суммарный отрицательный эффект, поэтому их растворение в воде должно сопровождаться ломкой водородных связей и, следовательно, понижением рефракции. [28]
 |
Концентрационная зависимость рефракций электролитов. [29] |
Ионы Li, Na, Ca2 и Sr2 обладают положительной гидратацией, ионы К, Rb, Ch, В г - и I - - отрицательной гидратацией. Сумма энергий ближней гидратации различных комбинаций ионов может быть как положительной, так и отрицательной и в результате растворение тех или иных солей может как укреплять, так и ослаблять водородные связи в воде. Конкретно соли калия, наиболее часто рассматриваемые в данной книге соединения, дают суммарный отрицательныii эффект, поэтому их растворение в воде должно сопровождаться ломкой водородных связей и, следовательно, понижением рефракции. Аналогично, хотя и в меньшей степени, должны понижать рефракцию при растворении в воде соли натрия. [30]
Страницы: 1 2 3 4