Ближняя гидратация
Cтраница 3
 |
Влияние магнитной обработки водных систем на химический сдвиг. [31] |
Искажение квазикристаллической решетки приводит к появлению большего числа мономерных подвижных молекул растворителя. Это соответствует представлениям О. Я. Самойлова об отрицательной ближней гидратации некоторых ионов. [32]
Наконец, наряду с подбором новых комплексообразующих реагентов нами было изучено и влияние природы катиона раствора азотнокислой соли, которым пропитывают хроматографическую бумагу. Это явление вполне удовлетворительно объясняется развиваемыми в структурной теории высаливания представлениями о ближней гидратации, положительной для лития и отчасти для натрия и отрицательной для калия и других более тяжелых щелочных металлов. Этот параметр может быть эффективно использован для повышения степени разделения в ряде систем, хотя в большинстве простых случаев и целесообразно использовать ионы аммония или реже натрия - ионы с малым гидратационным эффектом. [33]
Поэтому здесь целесообразно привести только те данные, которые опубликованы в самое последнее время. Интересно, что из теории высаливания, развитой Самойловым, вытекает следующая связь высаливания с ближней гидратацией аниона-высаливателя 129 ]: высаливание возрастает с усилением ближней гидратации аниона-высаливателя в случае высаливания слабо гидратирующихся катионов и уменьшается при высаливании катионов с сильной гидратацией. Основываясь на предложенной им теории высаливания, Самойлов нашел ИЗО ], что в присутствии катионов-высаливателей возможны также ситуации, когда для близких по свойствам ионов в вод-лых растворах наблюдаются максимальные различия в гидратации. [34]
Рассматривая связь гидрахных чисел с размерами ионов, автор работы [5] нашел, что гидратные числа приблизительно пропорциональны плотности электростатической энергии на поверхности иона. Там же [5] получено соотношение между h и радиусом сольватированного иона и впервые термодинамически обоснована зависимость ближней гидратации иона от его заряда и радиуса. Вместе с тем отмечается [66, 68], что уравнение (4.2) нельзя рассматривать как вполне удовлетворительное, так как концепция гидратных чисел является слишком большим упрощением. [35]
Наличие таких рядов указывает на значительную роль изменений в состоянии воды в водных растворах электро - - литов, а следовательно, и степени гидратации высаливаемых ионов под действием высаливающих. Наиболее подробно этот вопрос рассматривается в работах [9-13], в которых показано, что высаливание является результатом изменения ближней гидратации высаливаемого иона под влиянием катиона высаливателя и представляет собой суммарный эффект процессов обезвоживания и оводнения высаливаемых ионов. Эти процессы связаны с влиянием высаливаемых и высаливающих ионов на структуру воды. [36]
Поэтому здесь целесообразно привести только те данные, которые опубликованы в самое последнее время. Интересно, что из теории высаливания, развитой Самойловым, вытекает следующая связь высаливания с ближней гидратацией аниона-высаливателя 129 ]: высаливание возрастает с усилением ближней гидратации аниона-высаливателя в случае высаливания слабо гидратирующихся катионов и уменьшается при высаливании катионов с сильной гидратацией. Основываясь на предложенной им теории высаливания, Самойлов нашел ИЗО ], что в присутствии катионов-высаливателей возможны также ситуации, когда для близких по свойствам ионов в вод-лых растворах наблюдаются максимальные различия в гидратации. [37]
Именно с ближней гидратацией связаны так называемые кинематические свойства растворов и механизм протекания в растворах ряда процессов. Таким образом, напрашивается вывод, что гидратация ионов в водных растворах состоит не в связывании ионом большей или меньшей оболочки из молекул воды. Ближняя гидратация сводится лишь к более или менее сильному взаимодействию иона с ближайшими молекулами воды, число которых в разбавленных растворах определяется квазикристаллической структурой воды. [38]
Именно с ближней гидратацией связаны так называемые кинематические свойства растворов и механизм протекания в раст-вораьх ряда процессов. Таким образом, напрашивается вывод, что гидратация ионов в водных растворах состоит не в связывании иояом большей или меньшей оболочки из молекул воды. Ближняя гидратация сводится лишь к более или менее сильному взаимодействию иона с ближайшими молекулами воды, число которых IB разбавленных растворах определяется квазикристаллической структурой воды. [39]
Влияние ионов на структуру воды связано с их гидратацией. Различают ближнюю гидратацию ( взаимодействие иона с ближайшими к нему молекулами воды) и дальнюю гидратацию - поляризацию более отдаленных молекул воды. Характеристикой ближней гидратации является отношение времени пребывания молекулы воды в ближайшем окружении иона ко времени нахождения ее в положении равновесия с другими молекулами в невозмущенной структуре воды. На основании данных о растворимости солей и теплотах гидратации ионов установлено, что на связь одной молекулы с катионом в зависимости от его заряда ( 1, 2 или 3) приходится соответственно 42, 126 или 420 кДж / моль. В последнем случае гидратиро-ванный катион похож на химическое соединение. [40]
Влияние ионов на структуру воды связано с их гидратацией. Различают ближнюю гидратацию ( взаимодействие иона с ближайшими к нему молекулами воды) и дальнюю гидратацию - поляризацию более отдаленных молекул воды. Характеристикой ближней гидратации является отношение времени пребывания молекулы воды в ближайшем окружении иона ко времени нахождения ее в положении равновесия с другими молекулами в невозмущенной структуре воды. В последнем случае гидратированный катион похож на химическое соединение. [41]
Если ионы, входящие в состав соли, оказывают противоположно направленное действие, то суммарный эффект может быть различным в зависимости от того, влияние какого иона преобладает. Оказывает ли данная соль упорядочивающее или разрушающее действие на структуру воды, существенно зависит характер изменения свойств раствора при изменении концентрации и особенно температуры. От ближней гидратации зависят прежде всего кинетические свойства раствора ( связанные с движением ионов растворенного вещества и самих молекул воды): диффузия и самодиффузия, вязкость, теплопроводимость, электропроводимость. [42]
Теория высаливания из водных растворов, сформулированная О. Я. Самойловым [168, 169], обобщает изложенный материал. Рассматривая изменение ближней гидратации высаливаемого катиона в растворе под влиянием высаливателя, О. Я. Самойлов нашел, что основное значение имеет ориентация молекул воды вблизи высаливаемого иона и изменение ее под действием ионов высаливателя. Катионы высаливателя уменьшают, анионы увеличивают ближнюю гидратацию высаливаемого катиона. [43]
С ростом температуры за счет предразрушения структуры воды взаимодействие ионов с молекулами воды усиливается, и при ГГпредионы Na, К, Rb, С1 - и Вг из отрицательно гидратированных становятся положительно гидратированными. При Т Тпрея данный ион за счет компенсации разрушающего и стабилизирующего вкладов формально не оказывает влияния на структуру воды. Аналогичная ситуация складывается при рассмотрении влияния размеров ионов на характер их ближней гидратации. По мере роста ионного радиуса вклад разрушающего влияния возрастает, при значении г г пред сравнивается с упорядочивающим вкладом и при г / - рея начинает преобладать. Иными словами, можно сказать, что при г / пред происходит переход от положительно к отрицательно гидраггирующимся ионам. [44]
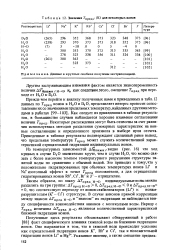 |
Значения Гпред ( К для некоторых ионов. [45] |
Страницы: 1 2 3 4