Гидрид - щелочной щелочноземельный металл
Cтраница 1
Гидриды щелочных и щелочноземельных металлов - это твердые соединения, связь в которых близка к ионной. Летучие водородные соединения В и элементов подгрупп IVA - VIIA газообразны; в них связь близка к ковалентной. [1]
Гидриды щелочных и щелочноземельных металлов представляют собой солеподобны. Так, чистый гидрид лития белого цвета, по часто он бывает слегка окрашен в голубовато-серым пвст примесями, например примесью металлического лития. [2]
Гидриды щелочных и щелочноземельных металлов являются одним из перспективных разовых источников водорода для автономных энергоустановок, изготовляемых на основе ЭХГ. [3]
Гидриды щелочных и щелочноземельных металлов - очень сильные восстановители, так как содержат отрицательно заряженные ионы водорода, которые легко отдают электроны. [4]
Гидриды щелочных и щелочноземельных металлов по своим свойствам сходны с соответствующими солями галогенов, отличаясь от последних своей неустойчивостью по отношению к воде. Состоят они из положительных ионов металла и отрицательных ионов водорода. При электролизе, например, расплавленного гидрида лития LiH на катоде выделяется литий, а на аноде - водород. Таким образом, водород можно отнести к элементам первой и седьмой групп. [5]
Гидриды щелочных и щелочноземельных металлов, - содержащие ион. [6]
Гидриды щелочных и щелочноземельных металлов гетеро-полярны. [7]
Гидриды щелочных и щелочноземельных металлов обладают солеобразной природой и представляют собой твердые кристаллические вещества. [8]
Гидриды щелочных и щелочноземельных металлов - это твердые соединения, связь в которых близка к ионной. Летучие водородные соединения бора и элементов подгрупп IVA-VIIA газообразны; в них связь близка к кова-лентной. [9]
Гидриды щелочных и щелочноземельных металлов представляют собой солеподобные вещества. [10]
Гидриды щелочных и щелочноземельных металлов получают путем непосредственного соединения элементов при нагревании. Способ этот в принципе очень прост, но для получения чистых продуктов нужно соблюдать ряд подчас трудно выполнимых условий. [11]
Гидриды щелочных и щелочноземельных металлов быстро разрушаются под действием влаги и кислорода воздуха, что иногда сопровождается самовозгоранием. Поэтому хранить их следует R запаянных ампулах, в атмосфере сухого водорода или инертного газа. [12]
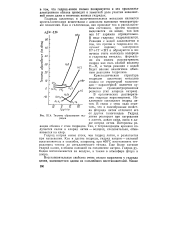 |
А. Теплоты образования гидридов. [13] |
Гидриды щелочных и щелочноземельных металлов являются кристаллическими веществами с довольно высокими температурами плавления. Как и галогениды, они проводят ток в расплавленном состоянии, причем водород выделяется на аноде, так как ион Н - заряжен отрицательно. В воде гидриды гидролизуются. Реакция с водой заключается в том, что протон и гидрид-ион получают поровну электронов Н Н - 2Н и образуются в конечном счете молекула водорода и гидроксид металла; формально мы можем рассматривать гидрид как соль слабой кислоты Н - Н, и тогда реакция с водой будет вполне аналогична обычным реакциям гидролиза. [14]
Гидриды щелочных и щелочноземельных металлов - бесцветные кристаллические вещества с высокими температурами плавления, термически устойчивые, связь в них близка к ионной. [15]
Страницы: 1 2 3 4