Гидрокарбонилирование
Cтраница 2
Высокое давление, как говорилось раньше, не ускоряет гидрокарбонилирования, но оно необходимо для предотвращения разложения активных карбонилов кобальта. При этом чем выше температура, тем большее давление должно ей соответствовать. Кроме того, следует учитывать, что в практических условиях процесса могут играть роль диффузионные факторы, а высокое давление способствует лучшей растворимости газов. Это особенно относится к гидрокарбонилированию низших газообразных олефинов, растворимость которых имеет прямое влияние на скорость процесса. С другой стороны, ограничения в давлении объясняются чрезмерными экономическими затратами на сжатие газов и изготовление аппаратуры высокого давления. [16]
В последующем изложении для этой реакции принимаются названия оксореакция или гидрокарбонилирование. Оптимальные условия оксо - и аналогичных реакций: температура 75 - 200, давление синтез-газа г 100 - 300 am; процесс проводят в присутствии кобальтового катализатора ( восстановленный металлический кобальт. При указанных оптимальных условиях в реакционной смеси могут одновременно присутствовать дикобальтоктакарбонил, гидрокарбонил кобальта и три-кобальтдодекакарбонил. [17]
Хотя из этой схемы и вытекает обратная пропорциональность между скоростью гидрокарбонилирования и парциальным давлением СО, она не дает простого объяснения зависимости скорости реакции от отношения водород: окись углерода. [18]
Методы декобальтизации, пожалуй, еще более разнообразны, чем методы гидрокарбонилирования. [19]
Термодинамические условия реакции в большей степени благоприятствуют гидрированию олефинов, чем гидрокарбонилированию. [20]
Важнейшим исключением в этом отношении является вариант процесса с применением взвеси катализатора, при котором стадии гидрокарбонилирования и гидрирования проводят на одном и том же катализаторе. В этом случае отпадает необходимость процесса декобальтизации. Кроме того, если установка предназначена для производства альдегидов в качестве целевых продуктов, то отпадает необходимость в стадии гидрирования. [21]
Любой механизм, предполагающий непосредственное соединение окиси углерода с олефином, опровергается обратной пропорциональностью между скоростью реакции гидрокарбонилирования и давлением окиси углерода. Реакция протекает в жидкой фазе; окись углерода передается олефину от промежуточного соединения, в котором она связана по крайней мере с одним атомом металла. [22]
Взаимодействие оле-фннов со вторичными спиртами в присутствии окиси углерода и карбонила кобальта дает возможность использовать водород спирта для гидрокарбонилирования олефина. [23]
Если оксосинтез проводят для получения спиртов в качестве целевого продукта, то частичное гидрирование альдегидов в спирты еще в стадии гидрокарбонилирования не имеет существенного значения. Однако если процесс проводят для получения альдегидов в качестве целевого продукта, то температуру реакции следует поддерживать возможно низкой, насколько это допускают требуемая скорость реакции и малая продолжительность контакта. [24]
В металлокомплексном катализе реакции окислительного шрисоединения представляют собой одну из стадий широко рас-шространенных реакций гомогенного гидрирования, карбонили - - рования, гидрокарбонилирования. [25]
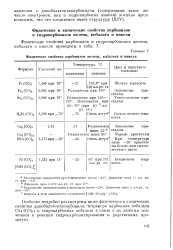 |
Физические свойства иарбонилов железа, кобальта и никеля. [26] |
Особенно подробно рассмотрены ниже физические и химические свойства дикобальтоктакарбонила, тетрамера карбонпла кобальта Со4 ( C0) i2 и гидрокарбонила кобальта в связи с их важным значением в реакции гидрокарбонилирования и родственных процессах. [27]
В отличие от зарубежной практики, использующей при производстве разветвленных кислот метод Коха, в СССР разработка процесса получения кислот осуществляется по следующим направлениям: 1) карбонилирование олефинов в присутствии серной кислоты; 2) теломеризация этилена низкомолекулярными кислотами в присутствии перекисного катализатора; 3) гидрокарбонилирование олефинов с последующей конденсацией и окислением полученных альдегидов. [28]
Гидрокарбонилирование ( гидрокарбоксилирование) проводят присоединением СО и Н2О к алкеиам, алкинам, арил ( алкил) галогенидам и тозилатам ароматич. [29]
Хотя непосредственное сравнение приведенных результатов затруднительно, так как опыты проводили не при одинаковых условиях, а анализы в каждом случае выполняли различными методами, из этих данных можно сделать некоторые выводы. При гидрокарбонилировании изомерных пентенов на восстановленных кобальтовых катализаторах выход спиртов, образующихся в результате присоединения к первому и второму углеродным атомам цепи, приблизительно одинаков. В присутствии дикобальтоктакарбонила как из 1 -, так и из 2-пентена образуется главным образом спирт нормального строения. [30]
Страницы: 1 2 3 4