Гидролиз - ион - металл
Cтраница 1
Гидролиз ионов металла приводит к подкислению среды, ускоряющему процесс коррозии, так как в кислой среде защитная способность пленок на поверхности металла снижается. [1]
Гидролиз ионов металлов, образующих гидроксиды с меньшей константой диссоциации, протекает более полно. [2]
Гидролиз ионов металла при ограниченной конвекции в объеме питтинга считают основной причиной увеличения в нем кислотности исходного раствора. Степень этой кислотности зависит от природы катиона. Следует ожидать, что в вершине трещины, развивающейся по границам зерен, содержащих фосфор, серу, углерод, карбиды и др. рН будет изменяться иначе, чем в трещине транскристаллитного типа. [3]
Гидролиз ионов металлов представляет собой протолитическую диссоциацию аквакомплексов, рассматриваемых как кислоты с основностью равной числу координированных металлом молекул воды. [4]
Учет гидролиза ионов металла, процесса анионного комплексооб-разования и ступенчатого образования комплексов с реагентом значительно усложняет выражения для коэффициента распределения. [5]
При гидролизе ионов металла иногда наблюдается такое же явление, как и в случае бериллия, а именно: вначале образовавшийся продукт гидролиза ВеОН в большей или меньшей степени полимеризуется, и поэтому функция образования становится зависимой от концентрации металла. Но этого не наблюдается в случае гидролиза солей магния и цинка [9], а также, вероятно, в растворах других образующих аммины одно - и двухзарядных ионов металлов, изученных в настоящей работе ( ср. [6]
Анализ явлений гидролиза ионов металлов лежит в основе гидролитической полимеризации и получения широкой группы неорганических клеев. [7]
Для предотвращения гидролиза иона металла измерения часто проводят с растворами, содержащими 0 1 М кислоты. Кроме того, концентрация водородных ионов часто не зависит от общей концентрации лиганда А. Это имеет место, например, в случае изучения хлоридных, бромидных и нитратных комплексов, где А является сопряженным основанием сильной кислоты. Если А - сопряженное основание слабой кислоты, то его концентрацию можно варьировать без изменения концентрации водородных ионов при условии, что лиганд вводится в систему в форме самой кислоты, а не одной из ее солей. Поэтому концентрации таких лигандов, как фторид - или сульфат-ионы, следует изменять добавлением различных количеств фтористоводородной кислоты или бисульфат-ионов HSOJ. В тех случаях, когда концентрация водородных ионов не зависит от значений qB и 21, уравнения ( 10 - 51), ( 10 - 53) и ( 10 - 54) можно применять к одной серии измерений, в которой исходная кислотность и концентрация вспомогательного лиганда поддерживаются постоянными, а изменяется лишь концентрация лиганда А. [8]
Ряд особенностей отличает гидролиз ионов металлов от гидролиза катионов типа аммония. Наиболее характерная из них состоит в том, что промежуточные частицы могут быть относительно нестойкими; в этом случае непригодны обычные допущения, применяемые в случае ступенчатой диссоциации многоосновных кислот. Другой, усложняющий дело фактор состоит в том, что гидроокиси или окиси многих металлов плохо растворимы, и выпадение осадка в щелочных растворах происходит даже при низких концентрациях ионов металлов. Однако наиболее неприятное обстоятельство заключается в том, что ионы многих переходных металлов образуют многоядерные гидроксокомплексы, содержащие несколько атомов металла, и уравнения, соответствующие условиям равновесия, нелинейны относительно аналитической концентрации иона металла. Все это усложняет математический подход к системам гидролизующихся ионов металлов. [9]
Повышение же рН вызывает гидролиз ионов высоковалентных металлов, однако только гидролизом нельзя объяснить их малую реакционную способность по отношению к металлохромным индикаторам. Известно также, что если раствор соли циркония содержит слишком много кислоты и его нейтрализуют сначала до рН 3 - 5, а затем подкисляют до рН 1, то после этого цирконий не реагирует с металлохромными индикаторами. [10]
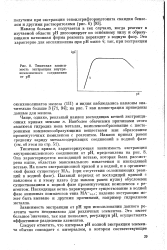 |
Типичная зависимость экстракции внутри-комплексного соединения от рН. [11] |
Наиболее обычными причинами этого являются гидролиз иона металла, комплексообразование с посторонними комплексообразующими веществами или образование промежуточных комплексов с реагентом. Наклон кривых равен среднему заряду металлсодержащих соединений в водной фазе ( см. об этом на стр. [12]
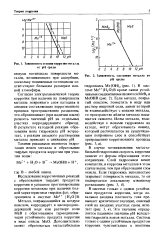 |
Зависимость степени коррозии металла от рН среды.| Зависимость состояния металла от рН среды. [13] |
Это значение определяется падением значения рН вследствие гидролиза ионов металла. [14]
Легко видеть, что при участии в гидролизе иона металла, являющегося ионом слабого основания, уравнения аналогичны. [15]
Страницы: 1 2 3 4