Гидролиз - ион - металл
Cтраница 2
Однако чрезмерное повышение рН раствора может привести к гидролизу ионов металлов и к выпадению в осадок не окси-хинолятов металлов, а основных солей или гидроокисей или к образованию смешанных осадков. Поэтому для каждого металла существует определенный интервал рН раствора, в пределах которого происходит наиболее полное осаждение данного металла в форме его оксихинолята. Ниже приводятся интервалы рН для наиболее полного осаждения оксихинолятов ряда металлов. [16]
С другой стороны, щелочные растворы также исключаются из-за гидролиза иона металла. Таким образом, оптимальная экстракция осуществляется в относительно узком интервале рН, причем пределы несколько увеличиваются при высоких концентрациях роданидов. Эта особенность роданидных экстракционных систем приводит к тому, что наиболее эффективна экстракция лишь из слабокислых растворов, а экстрагирующееся соединение представляет собой в действительности металлроданидную комплексную соль, а не кислоту. Однако, как и при экстракции металлгалогенидных соединений, природа экстрагирующегося соединения металла может изменяться с изменением условий и растворителей. [17]
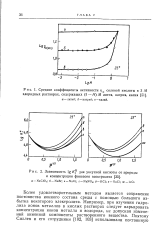
Экстракционный метод, по-видимому, весьма полезен при изучении моноядерного гидролиза ионов металлов. Это объясняется тем, что распределение ионов металлов при их очень низкой концентрации легко измеряется с помощью радиоизотопов, а гидролиз в водной фазе можно определить по изменению коэффициентов распределения с изменением концентрации ионов водорода. [18]
 |
Влияние рН на. [19] |
Основано оно на положениях так называемой гипотезы аналогий о сходстве реакций гидролиза ионов металлов и их реакции с органическими реагентами. [20]
В литературе имеется ряд работ, в которых представлены данные по гидролизу ионов металлов в различных средах. [21]
Информация о наиболее часто встречающихся случаях побочного комплексообразовання нонов металлов представлена в табл. 15.3. В этой таблице коэффициенты побочных реакций гидролиза ионов металлов представлены в виде lg aM L, отвечающего предполагаемому процессу присоединения ионов гндрокснла к нону металла. Напомним, что процесс гидролиза протекает как процесс отщепления протона от аква-нона металла, являющегося бренстедовской кислотой. Побочная реакция гидролиза нона металла может существенно изменить характер равновесия комплексообразовання ЭДТА с нонамн металла в растворе. Так, несмотря на то что комплексонат железа ( III) обладает высокой устойчивостью ( см. табл. 15.2), в растворах с рН Ш влияние гидролиза нонов железа ( III) настолько сильное, что его комплексонат будет разрушаться с образованием гндрокснда железа ( III) н свободного четырехзарядного аннона ЭДТА. [22]
При выводе этого уравнения, так же как и при выводе уравнений ( 6) и ( 7), делаются следующие допущения: а) отсутствует гидролиз иона металла; б) не образуется никаких полимерных молекул; в) не образуется никаких смешанных комплексов; г) любые комплексы между М и R образуются в водной фазе в незначительном количестве; д) в органической фазе единственным преобладающим соединением является MRn; e) концентрация соединения, обусловливающего маскирование, не зависит от рН, и число лигандов, присоединяющихся к иону металла с образованием растворимого в воде комплекса, не превышает четырех. [23]
Применение уравнений ( 14 - 15) - ( 14 - 20) ограничено тем, что они не учитывают конкурирующих реакций комплексообразования, в том числе гидролиза иона металла. [24]
Объясняется это довольно просто, если вспомнить, что иоиы металлов в водных растворах, в общем, подвергаются гидролизу, и здесь сказывается негативное влияние побочной реакции гидролиза ионов металла. [25]
Если осадителем служит бикарбонат, то благодаря диссоциации НСО3 - СО3 Н рН раствора будет меньше, чем при использовании в качестве осадителя карбоната, и, следовательно, уменьшится степень гидролиза ионов металла. [26]
Ион гидроксила имеет три неподеленные пары электронов и отрицательный заряд, что обусловливает его сильную тенденцию к комплексообразованию. Гидролиз ионов металлов с большим зарядом сопровождается образованием гидроксокомплексов. [27]
При рассмотрении влияния концентрации соли ионной среды, температуры раствора, давления и замены легкой воды на тяжелую, наблюдается тесная взаимосвязь между изменением структуры воды константой ее диссоциации и константой гидролиза ионов. Например, константы гидролиза ионов металлов уменьшаются при увеличении концентрации ионной среды. [28]
Следовательно, кажется целесообразным использовать ионную среду высокой концентрации, особенно, если требуется высокая концентрация ионов водорода или лиганда. В работах по гидролизу ионов металлов, например, часто нужно было использовать высокие концентрации ионов водорода для того, чтобы получить растворы, содержащие негидролизованные формы. [29]
Страницы: 1 2 3 4