Гидролиз - амидная связь
Cтраница 2
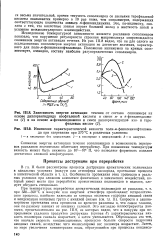
С в вакууме или инертной атмосфере преобладают гетеролитиче-ские процессы, наиболее важными из которых являются гидролиз амидной связи и конденсация концевых групп с амидной связью ( см. гл. Скорости и закономерности протекания этих процессов во времени различны и, что самое главное, они по-разному зависят от внешних условий. Это наглядно иллюстрируется данными, представленными на рис. II 1.9, из которых видно, что в вакууме при непрерывном удалении продуктов деструкции ( кривая 3) характеристическая вязкость полимеров сначала возрастает, а затем уменьшается. Обусловлено это тем, что вначале скорость конденсационных процессов больше скорости гидролиза амидных связей, вследствие чего молекулярный вес полимера возрастает. [17]
Хотя детали каталитического механизма действия пепсина все еще не ясны, хорошо известно, что гидролиз амидной связи подвергается эффективному нуклеофильному катализу близлежащей карбоксильной группой. Эта реакция весьма чувствительна к изменениям структуры. Гидролиз наиболее реакциоиноспособных соединений ( например, кислых амидов диметилмалеиновой кислоты ( 47), имеющих период полупревращения при 37 С менее 1 с) подчиняется общему основному катализу. [18]
 |
Кинетические кривые гидролитической полимеризации е-капролактама в присутствии 2 0 % ( масс. воды при разных температурах ( в С. [19] |
Первой стадией процесса по этой схеме является гидролиз амид-ной связи в лактаме, а третьей - гидролиз амидной связи в полимере. [20]
Замыкание цикла по методу Циглера и последующий гидролиз образующегося енамино-нитрила должны были привести к кетону 260, который, как ожидалось, после гидролиза амидных связей даст катенан. [21]
Это свойство имидазола играет центральную роль в деятельности некоторых ферментов, содержащих имидазольное кольцо гистидина, например пищеварительного фермента химотрипсина, который отвечает за гидролиз амидных связей пептидов в тонкой кишке: фермент переносит протон из одного положения в другое, что обеспечивается амбидентным характером имидазольного ядра. На приведенной ниже схеме показано, каким образом гетероцикл позволяет протону двигаться взад и вперед из одного положения в другое через гетероцикл. [22]
В настоящее время известны основные механизмы биодеградации пестицидов в водоносном пласте. Гидролиз амидной связи, характерный для фениламидных соединений, фенилмочевин, фенилкарбаматов, практически не идет до конца и заканчивается образованием хлорированных анилинов. При гидролизе эфирных связей фенилкарбаматов также образуются анилины. Гидролиз фосфорорганических пестицидов сопровождается образованием окснпроизводных, в том числе оксианилинов. Накоплением метаболитов в подземных водах завершаются процессы дегалогениро-вания, характерные для пестицидов класса хлорированных углеводородов. Так, образование ДЦД является результатом восстановительного дегало-генирования ДЦТ. Накопление ДЦЕ и 7 - 23 4 5 6 - пентахлорциклогексена4 происходит в результате дегидрогалогенирования ДЦТ и линдана соответственно. Первичным процессом деградации пестицидов, имеющих ароматические ядра и алкильные радикалы, является гидроксилирование. [23]
Связи углерод - азот в амидах органич. Гидролиз амидной связи в белках катализируется также протоолитич. При действии растворов иеорганич. [24]
 |
Гидролиз цефалоспорина С. [25] |
Пенициллиназы ( ( З - лактамазы) гидролизуют р-лактамное кольцо молекулы субстрата и являются основой устойчивости болезнетворных бактерий к пенициллинам и цефалоспоринам. В результате гидролиза амидной связи кольца образуется пе-еициллиновая кислота ( рис. 4.9), которая полностью лишена антимикробной активности. [26]
Амидные группы гидролизуются водой при 160 - 180 С ( с образованием новых активных групп МН2 и СООН, а в присутствии ионов Н или ОН - даже при низких температурах. Ионы Н катализируют гидролиз амидных связей, если между соседними группами CONH находится не менее 3 - 4 метиленовых групп, а ионы ОН - катализируют гидролиз тех же групп, разделенных 1 - 2 углеродными атомами. [27]
В качестве примера такого ферментативного разделения рассмотрим расщепление () - лейцина при помощи фермента ацилазы, выделенного из почек свиньи. Этот фермент катализирует гидролиз амидных связей ь-аминокислот, но не в-аминокислот. [28]
Они устойчивы к действию минеральных масел и жиров, воды, грибков, бактерий и плесени. Вода и щелочь вызывают гидролиз амидной связи лишь под давлением и при высокой температуре. [29]
Большое влияние на гидролизуемость полиамидов оказывает их химическое строение. Как показал Стертевант [91], гидролиз амидных связей значительно экзотермичнее гидролиза пептидных. Соответственно наиболее устойчивы к гидролизу полиамиды из а-аминокислот. Так, после полного омыления карбобензоксигрупп у поли-п - М - карбобенз-оксиаминофенилаланина действием концентрированной бромистоводородной кислоты Села и Качальский [85] нашли, что амидные связи в цепи макромолекулы еще не разрушены. При омылении этилового эфира полиаминомалоновой кислоты Френкель и другие исследователи [92] показали, что омыляются только боковые зтоксильные группы, а амидные связи в цепи полимера не затрагиваются. Вайда и Брукнер [93] установили, что полиаспарагиновобензи-ловый эфир может быть легко омылен по эфирной связи в свободную поликислоту, амидные группы которой при этом не омыляются. [30]
Страницы: 1 2 3 4