Гидролиз - амидная связь
Cтраница 3
Полиамиды не являются реакционноспособными соединениями, поскольку большая часть их макромолекул состоит из химически инертных углеводородных цепей и только амидные группировки и концевые амино - и карбоксильные группы, число которых сравнительно невелико, вступают в химические реакции. Прежде всего среди реакций полиамидов следует отметить гидролиз амидных связей при повышенных температурах. Ранее уже отмечалось, что путем гидролиза осуществляется регенерация отходов полиамидов и волокон на их основе. В присутствии кислот и щелочей гидролиз полиамидов значительно ускоряется. [31]
Установлено, что инсектицидные производные мочевины типа дифлубензурона в различных объектах разлагаются. Процесс разложения идет через гидроксилирование ароматического ядра и гидролиз амидной связи [158 - 163]; эти процессы могут протекать одновременно или последовательно. Дальнейшее разрушение образующихся продуктов протекает по обычной схеме, характерной для ароматических аминов. Дифторбензой-ная кислота разлагается медленно. [32]
Амиды и амидины содержат реакционноспособные связи и подвергаются различным реакциям разложения в зависимости от строения индивидуальных соединений. Многочисленными исследованиями доказано, что основным процессом является гидролиз амидной связи, в результате которого образуются соответствующие амины ( анилины) и карбоновые кислоты. Производные мо-нохлоруксусной кислоты [12] дают при последующем замещении атома хлора на гидроксильную группу глиоксиловую кислоту, которая вовлекается в естественный обмен веществ. [33]
Процесс деструкции полиамидов значительно ускоряется при контакте с влагой. В условиях повышенной температуры или давления в присутствии воды происходит гидролиз амидной связи, сопровождающийся деструкцией основных - цепей полимера. При больших дозах гамма-излучений уменьшается степень кристалличности полимеров, нарушается регулярность строения главных цепей, снижается механическая прочность и износостойкость. Добавление ароматических аминов, эпоксидных смол и графита способствует повышению устойчивости полиамидов к действию излучений. [34]
Специфичность ферментов проявляется также и в отношении условий реакции. Так, например, одна и та же реакция - гидролиз амидной связи в пептидах - ускоряется химотрипсином при значениях рН, близких к нейтральным, тогда как другая протеаза - пепсин - функционирует только в кислой среде. [35]
Поэтому важное практическое значение имеет соотношение содержания воды на первых и последних стадиях полиамидирования, обеспечивающее проведение всего процесса за Минимальное время. Предусматривается своевременное удаление воды из сферы реакции с целью торможения процесса гидролиза амидных связей и достижения высокой степени полимеризации. Однако это может привести к образованию полимера с увеличенной средней молекулярной массой, который не может быть использован для формования волокна. Для того, чтобы получить полимер такой молекулярной массы, нужно вовремя прервать процесс амидирования. Для этого применяют реагенты, ограничивающие ( регулирующие) степень полимеризации, которые называют регуляторами. Их добавляют в капролактам вместе с активаторами перед загрузкой в аппарат для полиамидирования. В качестве регуляторов могут быть использованы вещества, способные присоединяться к одной или обеим концевым группам поликапроамида и блокировать их. [36]
Синтез и гидролиз белковых молекул ( а некоторые белки уже синтезированы in vitro) требует особых методов. Но прежде всего остановимся в настоящем разделе на классическом синтезе амидов и гидролизе амидной связи, тем более что амиды являются важными производными карбоновых кислот. [37]
Страус и Уолл предположили, что важная роль в процессах термодеструкции полиамидов принадлежит небольшим количествам воды, которая удерживается в материале и вызывает гидролиз амидных связей, после чего происходит выделение углекислоты в результате декарбоксилирования образующихся свободных карбоксильных групп. [38]
В водной среде пропанид разлагается под действием солнечного света. При этом происходят: замещение атомов хлора на гид-роксильные группы, приводящее к образованию моно - и диокси-пропионанилидов; отщепление ароматического ядра с образованием амида пропионовой кислоты; восстановительное дехлорирование пропанида с образованием 3-хлор - или 4-хлорпропионанилида, а также незамещенного пропионанилида; гидролиз амидной связи с образованием 3 4-дихлоранилина и тетрахлоразобензола; окисление диоксипроизводных пропанида с конденсацией в полимерные соединения типа гуминовых кислот. Процесс фотолиза пропанида наблюдали также в опытах, проведенных в полевых условиях [38]; пониженная инсоляция способствует значительному накоплению остатков токсикантов в растениях риса. При фотолизе хлордиме-форма в первую очередь отщепляются метальные группы при атоме азота ( см. схему на с. Образующиеся форманилиды подвергаются дальнейшему распаду. [39]
Полиамиды представляют собой твердые роговидные непрозрачные продукты от белого до светло-желтого цвета. Реакционная способность полиамидов невелика. Наиболее известной реакцией является гидролиз амидных связей. Вода при температуре до 100 С не действует на амидные связи даже при длительном контакте, но при 150 С и выше под давлением может вызвать полный гидролиз. Щелочи лишь немного эффективнее - воды, но кислоты заметно гидролизуют полиамиды. [40]
Херманс [342], на основании изучения полимеризационного равновесия при полимеризации е-капролактама в присутствии воды, отмечает, что с увеличением количества воды уменьшается выход полимера и растет содержание мономера и циклических олигомеров. Реакционноспособность концевых групп не зависит от величины молекулярного веса. Существенную роль, кроме гидролиза амидной связи и обратного ее образования, играет реакция присоединения е-капролактама к концам полимерной цепи. [41]
В качестве примера можно привести трипсин - фермент, синтезируемый поджелудочной железой и секретируемый в кишечник. Будучи протеолитическим ферментом, он гидролизует пептидные связи, образованные карбоксильной группой аргинина или лизина. Кроме того, трипсин катализирует гидролиз амидных связей ( это было установлено при работе с синтетическим субстратом бензоил - L-аргининамидом), а также гидролизует сложноэфирные связи между аминокислотой и спиртом. [42]
Кинетические данные для ыс-изомера дают линейную зависимость Лайнуйвера - Берка, что также подтверждает образование комплекса. Дальнейшие доказательства образования комплекса были получены на основании изучения фазовой диаграммы растворимости. Возможность равновесного образования комплекса с последующим внутримолекулярным гидролизом амидной связи по механизму нуклеофилыюго общего кислотного катализа, безусловно, стимулирует дальнейшие исследования. [43]
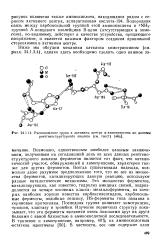 |
Расположение групп в активном центре ос-химотрипсина по данным рентгеноструктурного анализа ( текст [ 46а ]. [44] |
Возможно, единственным наиболее важным заключением, полученным на сегодняшний день из всех данных рентгеноструктурного анализа ферментов является тот факт, что каталитический участок, обнаруженный в химотрипсине, характерен также для других ферментов. Всегда существовала надежда, возможно даже разумное предположение того, что не все из множества ферментов, катализирующих данную реакцию, используют разные каталитические механизмы. Это множество ферментов, катализирующих, как известно, гидролиз амидных связей, подразделяется на четыре основных класса: металлоферменты, из которых наиболее хорошо известна карбоксипептидаза, карбоксильные ферменты, подобные пепсину, HS-ферменты типа папаина и сериновые протеиназы. Последняя группа включает химотрипсин, трипсин, эластазу и тромбин. Изучение первичных структур показывает, что эти ферменты являются очень похожими друг на друга белками с явной близостью в аминокислотной последовательности. [45]
Страницы: 1 2 3 4