Гидролиз - пептидная связь
Cтраница 3
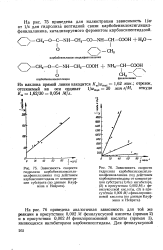
На рис. 75 приведена для иллюстрации зависимость 1 / ш от 1 / 5 для гидролиза пептидной связи карбобензилоксиглицил-фенилаланина, катализируемого ферментом карбоксипептидазой. [32]
Если препараты карбоксипептидазы содержат слишком много примеси эндопептидазы, то предварительная инкубация с ДИПФФ не исключает возможности гидролиза других пептидных связей. В таких случаях рекомендуется перекристаллизовать фермент. [33]
Аг ] - концентрация остатков аминокислот; [ Р ] - концентрация полипептидов; / q - константа скорости гидролиза внутренних пептидных связей, приводящего к образованию новых полипептидов. [34]
Молекула белка-фермента узнает молекулу субстрата или некоторую ее часть, как, например, в случае протеолитических ферментов, катализирующих гидролиз пептидных связей. Узнавание выражается в образовании реакционного комплекса со специфическим субстратом. Комплексы с ингибиторами и активаторами, с аллостерическими эффекторами также возникают в результате специфического узнавания. В узнавании участвуют непосредственно активный центр фермента, включающий и соответствующий кофактор, и косвенно вся белковая глобула. [35]
Аналогичные превращения протекают в реакциях свободных аминогрупп концевых аминокислот в пептидах и белках, например, с 2 4-динитрофторбензолом; при гидролизе пептидных связей [8] образующиеся динитрофениловые кислоты можно идентифицировать. [36]
При фотохимическом разрушении шерсти под действием света и атмосферных условий происходит разрыв дисульфидных связей, отщепление серы и ее окисление до сернистой и серной кислот, ускоряющих гидролиз пептидных связей. Все это влечет за собой понижение прочности волокна. [37]
Для определения числа дисульфидных связей в белке требуется: 1) восстановить днсульфидные связи до меркаптогрупп, 2) получить производные этих групп с ДТНБ, 3) провести гидролиз пептидных связей, 4) измерить количество образовавшегося производного ДТНБ. Каким еще операциям следует подвергнуть белок для того, чтобы точно определить число дисульфидных связей в нем. [38]
При более высокой температуре ( 30 - 35) действие пепсина, фи-цина и проназы приводит к большему или меньшему разрушению тройной спирали макромолекулы коллагена, связанному, по-видимому, с гидролизом пептидных связей. Проназа даже при 20 вызывает укорачивание молекулы коллагена с ее А-конца приблизительно на 5 %, после чего молекула становится особенно чувствительной к действию других протеаз. Действие трипсина на коллаген при всех условиях крайне ограничено. [39]
Принципы и критерии, принятые в настоящей статье для анализа химических реакций белков, в значительной степени основаны на принципах и методах, предложенных в появившихся почти одновременно фундаментальных обзорах Херриотта [18] и Олькотта и Фрегакель-Коярата [19] - В этой статье будут рассматриваться только неионные реакции, которые затрагивают главные связи боковых цепей аминокислот. Гидролиз пептидной связи и простые процессы ионизации из рассмотрения исключаются. Конечно, денатурацию можно вызвать также жесткой обработкой при помощи белковых реагентов, но основное внимание будет уделено реакциям, протекающим в мягких условиях и не Приводящим к необратимым структурным изменениям. [40]
Имеется большое сходство между рассмотренной реакцией ( а) и многочисленными реакциями гидролиза пептидов. При гидролизе пептидной связи наблюдается реакция разрыва одной из связей в пептидной группе, однако механизм реакции полностью не изучен. [41]
Последний пептид состоит преимущественно из основных аминокислотных остатков ( 8 остатков лизина и 4 остатка аргинина) и называется ингибитором пепсина. Пепсин катализирует гидролиз пептидных связей, образованных аминогруппами ароматических аминокислот ( фенилаланин, тирозин), а также аспарагиновой, глутаминовой кислот, лейцина и пар ала-ала, ала-сер. Фермент створаживает молоко, т.е. растворимый казеиноген в присутствии ионов кальция переводит в нерастворимый казеин. Его продвижение по пищеварительному тракту замедляется, что увеличивает время действия протеиназ. [42]
Строение веществ, вовлеченных в химические реакции, определяет скорость каталитического процесса. Например, гидролиз пептидной связи под действием протеиназ происходит с различной скоростью, зависящей от строения конкретной белковой макромолекулы, вовлеченной в реакцию. [43]
Каждый из этих ферментов атакует вполне определенные пептидные связи. Трипсин катализирует гидролиз пептидных связей, карбонильная группа которых принадлежит одной из основных аминокислот, обычно аргинину или лизину. Пепсин и химотрипсин предпочтительно катализируют гидролиз тех пептидных связей, в образовании которых участвуют ароматические аминокислоты, в частности триптофан, тирозин и фенилаланин. Среди протеолитических ферментов наиболее высокой специфичностью обладает трипсин; поэтому именно он наиболее подходит для такого рода анализа. Ясно, однако, что при помощи только одного, пусть даже абсолютно специфичного, фермента невозможно определить полную последовательность аминокислот в полипептиде. Если, например, триптическое расщепление полипептида дало пять фрагментов ( пептидов), в сумме соответствующих всей цепи, и если даже для каждого из них удалось установить аминокислотную последовательность, то это еще не все; требуется узнать, в каком порядке эти пептиды располагались в нативном полипептиде. Чтобы узнать это, необходимо получить другие пептиды, которые перекрывались бы с первыми. Главное преимущество ферментативного гидролиза - специфичность реакции расщепления в отношении природы расщепляемых пептидных связей - накладывает в то же время строгое ограничение на применимость этого метода. В идеале желательно было бы, например, иметь возможность расщеплять иногда те пептидные связи, которые в норме трипсином не атакуются, или, наоборот, предохранять от расщепления связи заведомо чувствительные. Недавно были предложены некоторые модификации методики, которые позволяют в какой-то мере решить эту задачу. [44]
Последние ферменты обладают более широкой специфичностью. Химотрипсин катализирует гидролиз пептидных связей, образованных карбоксильными группами ароматич. С меньшей скоростью гид-ролизуются связи лейцина, метиоиина и гистндина. [45]
Страницы: 1 2 3 4