Гидролизат - белок
Cтраница 2
Количественное определение аминокислот в гидролизате белка или пептида проводится с помощью аминокислотного анализатора - прибора, разработанного в 1958 г. С. [16]
Число пептидов, выделенных из гидролизатов белков, в настоящее время измеряется сотнями. Во многих случаях была установлена структура выделенных пептидов, некоторые из них. [17]
Двумерное разделение пептидов, например гидролизатов белков, на целлюлозных и силикагелевых пластинках, где в одном ( чаще первом) направлении используется электрофорез в тонком слое ( ТСЭ) при кислом рН буфера, а во втором - распределительная ТСХ. Оно применяется как для целей идентификации и сопоставления родственных белков ( например, для выявления мутационных или патологических изменений), так и в качестве препаративного метода для последующего анализа аминокислотной последовательности в пептидах. [18]
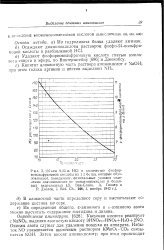
Описано фракционирование радиоактивно меченных пептидов трипсинового гидролизата белка на колонке Spherisorb ODS ( 0 46 X 25 см) линейным градиентом ( 0 - 62 5 %) этанола в 4 5 % - ном растворе НСООН. В растворах с высоким содержанием этанола ( как и ацетонитрила) растворимы не все пептиды. Хроматографию труднорастворимых пептидов иногда удается осуществить, используя в качестве органического растворителя пропанол. Относительно высокая вязкость пропанола заставляет снижать скорость элюции, но для крупных пептидов это все равно необходимо делать ввиду их замедленной диффузии. [19]
Для разделения 11 аминокислот в гидролизатах белков, предназначенных для вливаний, предложены следующие растворители [107]: грег-амиловый спирт - метилэтилкетон - вода ( 6: 2: 2) - в одном направлении; изопропиловый спирт - 99 % муравьиная кислота - вода ( 20: 1: 5) - в другом направлении. [20]
Для количественного анализа аминосахаров в гидролизатах белков наиболее пригодным является формазановый метод. [21]
Фактор, роста найден также в гидролизатах очищенных белков, что указывало на пептидную природу активного начала. [22]
Основы метода, а) Из - гидролизата белка удаляют аммиак. [24]
Нет сомнения в том, что из гидролизатов белков могут быть получены высокоочищенные L-аминокислоты. Тем не менее продажные препараты аминокислот зачастую загрязнены аминокислотными примесями, которые могут быть источником экспериментальных ошибок. В связи с этим микробиологи при приготовлении сред для определения аминокислот посредством бактерий нередко предпочитают применять синтетические DL-аминокислоты, а не L-изомеры, выделенные из белковых гидролизатов. Можно привести следующие примеры часто встречающихся загрязнений: в полученных из белков препаратах лейцина и глутаминовой кислоты часто содержатся метионин, а в препаратах глутамина - аргинин и аспарагин; препараты триптофана бывают загрязнены тирозином, а препараты тирозина - цистином. Выделенный из гидролизатов изолейцин обычно содержит лейцин, и наоборот. [25]
Для разделения смеси аминокислот, находящихся в гидролизате белка, и качественного обнаружения отдельных аминокислот широко используется метод распределительной хроматографии на бумаге. [26]
 |
Определение аминокислот. [27] |
Это свойство используют для определения пролина в гидролизатах белков. Сухой остаток обрабатывают одновременно 4 мл 3 % - ного раствора трихлоруксусной кислоты и 1 мл 10 % - ного раствора фосфорномолибденовой кислоты ( для удаления пептонов) и фильтруют. Отбирают 0 5 мл фильтрата, вводят 0 5 мл 2 % - ного водного раствора нингидрина и нагревают 10 мин при 100 С. После охлаждения добавляют 50 мл воды и экстрагируют продукт реакции 10 мл изобутилового спирта в течение 3 мин. Верхний слой отделяют и измеряют оптическую плотность при 533 нм. [28]
Для удаления минеральных кислот и дикарбоновых аминокислот из гидролизатов белков целесообразно фильтровать гидролизат через систему колонок, в которой чередуются секции с катионитами ианионитами. Этим создаются и более благоприятные условия для фракционирования других компонентов смеси. [29]
Часто перед исследователями встает задача селективного выделения из суммарного гидролизата белка пептидов, несущих определенные функциональные группы. Для этих целей может быть эффективно использована хемоспецифическая, или ко валентная, хроматография, основанная на образовании ко валентной связи пептида с носителем. Чаще всего метод ковалентной хроматографии применяют для селективного аыделения иистеинсодержащих пептидов. При этом пептиды, не содержащие остатков цистеина, не саязываются с носителем и удаляются при промывании соотаетстаующим буфером. Цистеинсодержащие пептиды выделяют далее восстановлением дисульфидных связей при рН 8 0 избытком меркаптоэтанола или дитиотреита. Более селективного разделения тиолсодержащих и тиолнесодержащих пептидов можно достигнуть, если проводить ферментативный или химический гидролиз белка, предварительно иммобилизованного иа нерастворимом носителе. В качестве носителя в обоих случаях используется тиол-сефароэа 4В, которая содержит в качестве активированной группы смешанный дисульфид, образующийся при обработке глу-татион-сефарозы 2 2 -дипиридилдисульфидом. [30]
Страницы: 1 2 3 4