Осажденная гидроокись
Cтраница 1
Осажденные гидроокиси редко бывают чистыми, чаще всего вследствие адсорбции ими посторонних веществ. [1]
Осажденную гидроокись никеля растворяют в избытке титрованной кислоты; избыток кислоты оттитровывают по метилоранжу. [2]
Они исследовали как осажденную гидроокись, так и бруцит, причем условия были выбраны так, чтобы исключить торможение диффузии паров воды продуктом. [3]
При добавлении к раствору свеже осажденной гидроокиси алюминия происходит коагуляция масла. Скоагулировавшее масло извлекают из осадка органическим растворителем. [4]
Активность медного катализатора, приготовленного из осажденной гидроокиси, является функцией температуры осаждения. [5]
Действительно, для образования ионов Zr4 после растворения осажденных гидроокисей достаточно десятикратного количества алюминия. Так как алюминий не мешает взаимодействию циркония с арсеназо. [6]
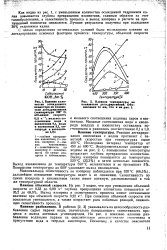
Как видно из рис. 1, с уменьшением количества осажденной гидроокиси калия повышается глубина превращения изопентана, главным образом за счет газообразования, а селективность процесса и выход изопрена в расчете на пропущенный изопентан снижаются. Лучшие результаты получены при осаждении-30 % гидроокиси калия. [8]
Для этой цели от окиси скандия, полученной после прокаливания осажденной гидроокиси ( однократное отделение), отбирали 1 0 мг и определяли в этом количестве примесь окислов редкоземельных металлов рентгеноспектральным методом. [9]
При приготовлении металлических катализаторов без носителя окислы часто получают дегидратацией осажденных гидроокисей. Для нанесенных образцов иногда используют метод осаждения гидроокиси на носителе, но в случае образцов с высокой поверхностью и развитой внутренней пористостью это сделать не просто. [10]
Иногда повышение растворимости осадков при добавлении большого избытка осадителя бывает обусловлено амфотер-ностью осажденных гидроокисей ( Al ( OH) 3, Zn ( OH) 2 и др.), или образованием кислых солей. Кроме того, чрезмерный избыток осадителя вызывает усиление солевого эффекта, всегда повышающего растворимость осадков. [11]
Сабатье и Мейль [359] указывают, что окись железа, полученная дегидратацией осажденной гидроокиси при температуре ниже 350, является гораздо более активным катализатором для спиртов, чем полученная при красном калении. Сабатье [357] объясняет это тем, что катализ зависит от величины поверхности; поэтому аморфные окиси, полученные из осажденных гидроокисей, дегидратированных при низких температурах, гораздо более активны, чем кристаллические окиси или окиси, подвергшиеся спеканию или обжигу при красном калении. После обжига часто получается гораздо меньшая поверхность для молекулярной конденсации. Это особенно верно в отношении окисей металлов с малыми атомными весами, например алюминия, железа, кремния и хрома. [12]
Иногда повышение растворимости осадков при добавлении большого избытка осадителя бывает обусловлено амфотерностыо осажденных гидроокисей А1 ( ОН) 3, Zn ( OH) 2 и др. или образованием кислых солей. Кроме того, чрезмерный избыток осадителя вызывает солевой эффект и растворимость осадков повышается. [13]
Иногда повышение растворимости осадков при добавлении большого избытка осадителя бывает обусловлено амфотерностью осажденных гидроокисей А1 ( ОН) 3, Zn ( OH) 2 и др. или образованием кислых солей. Кроме того, чрезмерный избыток осадителя вызывает солевой эффект и растворимость осадков повышается. [14]
Это соединение было получено синтетически в твердой фазе, а также при кипячении осажденных гидроокисей; оно кристаллизуется в кубической - системе и имеет красно-коричневый цвет с фиолетовым оттенком. [15]
Страницы: 1 2 3 4